哺乳动物雷帕霉素靶蛋白(mTOR)参与各种细胞功能的调节,并且与心血管疾病(CVDs)的发展密切相关。mTOR是PI3K相关激酶家族中的丝氨酸/苏氨酸蛋白激酶,可以形成两种不同的多蛋白复合物,mTORC1和mTORC2来行使不同的功能。mTORC2参与细胞存活,细胞骨架重塑和细胞迁移的调节。Rictor是mTORC2的核心成分,在调节免疫细胞中发挥重要作用。此外,具有内皮Rictor敲除的小鼠表现出胚胎致死性,并且有条件地敲除内皮Rictor显著降低了成纤维细胞生长因子诱导的小鼠新生血管形成。然而,关于Rictor对内皮结构或功能的影响的研究通常缺乏。
内皮完整性丧失或内皮功能障碍被认为是心血管疾病的诱发因素,例如高血压。血管内皮的结构完整性取决于内皮细胞(ECs)之间的细胞连接。粘附连接(AJs)是细胞连接的主要类型。血管内皮钙粘蛋白(VE-cadherin)是AJs的主要蛋白质成分。
在血管的分支和分叉处,ECs受到振荡剪切应力或低剪切应力(LSS)的刺激。在这里,内皮稳态不平衡,容易发生动脉粥样硬化。相反,在直血管区域,观察到单向血流,生理剪切应力(PSS)对血管内皮具有保护作用。然而,在剪切应力条件下,Rictor在内皮完整性和血管内皮钙粘蛋白表达中的作用缺乏研究。
血管性血友病因子(VWF)是内皮稳态的另一个关键标志物。mTOR激酶抑制剂可以在不影响细胞内VWF分泌的情况下抑制血栓形成。然而,尚未报道VWF和Rictor在内皮损伤中的关系。
在南京医科大学第一附属医院心血管内科、南京医科大学附属江宁医院重症科的一项研究中,验证了Rictor在生理稳态下对内皮完整性的影响,以及LSS诱导的血管内皮损伤下对VE-钙粘蛋白和VWF表达的影响。

Rictor 缺失破坏了层流区域的内皮完整性
在成功生成内皮Rictor缺失小鼠模型后,实验选择了Rictorfl/fl 和 RictoriΔEC 小鼠胸主动脉检测内皮形态,其中内皮细胞暴露于PSS(15 dyn/cm2)。结果显示,Rictor缺失后内皮完整性受损(图1)。以上结果表明,内皮Rictor缺失可导致内皮完整性丧失。

图1 Rictor 缺失破坏了胸主动脉区域的内皮完整性。
图像显示Rictorfl/fl (上)和 RictoriΔEC (下)小鼠胸主动脉内皮的形态。从左到右的红色框区域是局部放大区域,黑色箭头表示流向。
Rictor 缺失破坏了左颈总动脉区域的内皮完整性并扩大了细胞连接
为了在体内病理状态下模拟LSS(2 dyn/cm2),在小鼠中部分结扎左颈总动脉(LCA),右颈总动脉(RCA)未结扎。结果显示,LCA血管内皮受损,RictoriΔEC 小鼠表现出更明显的内皮形态损伤。此外,LSS刺激使细胞连接变宽,RictoriΔEC 小鼠的LCA细胞连接间隙更明显。以上结果表明,Rictor的缺失参与了LSS引起的血管内皮损伤的病理过程。
Rictor 缺失促进应力纤维形成
接下来探讨了Rictor缺失加重LSS诱导的血管内皮形态损伤的机制。F-肌动蛋白是内皮细胞连接复合物的重要组成部分。F-肌动蛋白以完整和连续的形式位于细胞膜的外围,并与 VE-钙粘蛋白复合物结合形成线性 AJs 以维持内皮屏障功能。
实验在体外模拟了平行板流动室系统中不同类型剪切应力对HUVECs的刺激。结果显示,在PSS条件下,F-肌动蛋白主要均匀分布在细胞周围。用LSS刺激HUVECs 1h后,F-肌动蛋白的极性受到干扰。观察到明显的应力纤维形成。在LSS条件下沉默Rictor后观察到增强的应力纤维形成(图2 A、B)。这一发现表明,Rictor对细胞骨架蛋白的排列很重要,表明Rictor可能通过调节F-肌动蛋白的分布和排列参与LSS诱导的ECs的形态变化。
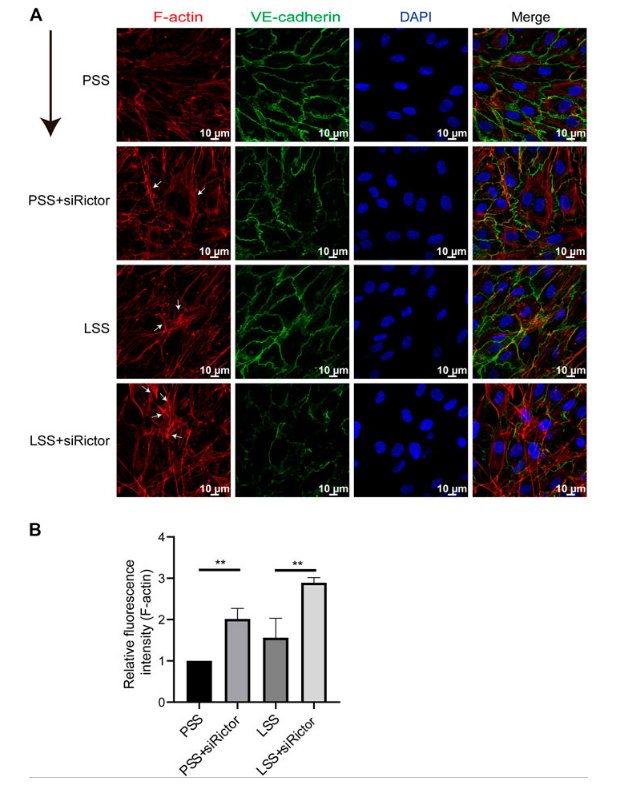
图2 Rictor参与了剪切应力下细胞骨架的排列。
(A)免疫荧光图像显示了由LSS刺激和有或没有Rictor siRNA转染的肌动蛋白丝(F-肌动蛋白)的极性。(B)测量F-肌动蛋白的平均荧光强度。
低剪切应力引起的粘附连接断裂
内皮 AJs 在维持内皮完整性方面起着关键作用。在体外,观察到AJs的主要蛋白VE-钙粘蛋白的表达和定位。在PSS刺激下,VE-钙粘蛋白主要位于细胞膜上,细胞连接处染色清晰光滑。然而,在LSS刺激下,VE-钙粘蛋白部分转移到细胞质中,细胞连接处的锯齿状减小。此外,细胞间隙明显形成(图3 A)。通过免疫印迹检测HUVECs中的VE-钙粘蛋白表达。LSS导致VE-钙粘蛋白膜蛋白表达降低(图3 C),而总蛋白表达不变(图3 B)。上述结果表明,在LSS暴露期间,VE-钙粘蛋白在AJs的稳定性降低,随后VE-钙粘蛋白易位。

图3 LSS促进了VE-钙粘蛋白的易位。
(A)免疫荧光显示VE-钙粘蛋白在不同类型剪切应力下的定位。VE-钙粘蛋白在LSS刺激后在膜上的定位较少。右图显示了细胞间隙的定量。(B)在不同类型的剪切应力下检测总VE-钙粘蛋白表达。(C)在不同类型的剪切应力下检测细胞膜上VE-钙粘蛋白的表达。
下调Rictor降低低剪切应力刺激下血管内皮-钙粘蛋白表达及其膜定位
接下来,Rictor是否通过VE-钙粘蛋白影响ECs的完整性。在体外验证Rictor siRNA的转染效率。用Rictor siRNA转染HUVECs,然后用PSS或LSS刺激1小时。免疫印迹显示,在LSS刺激下,下调Rictor抑制VE-钙粘蛋白表达。在体内,RictoriΔEC小鼠的LCA中总VE-钙粘蛋白和VE-钙粘蛋白在细胞膜上的定位降低。以上结果表明,Rictor缺失加剧了LSS刺激的HUVECs中VE-钙粘蛋白的内化和重塑以及F-肌动蛋白,这是导致内皮形态损伤的重要机制。
低剪切应力促进内皮细胞中血管性血友病因子的表达
VWF是另一种调节血管内皮稳态的关键蛋白,其表达在不同剪切应力刺激下发生变化。在体内,与Rictorfl/fl 小鼠的RCA相比,VWF在LCA中上调。在体外,LSS刺激后VWF显著上调。上述数据表明,LSS上调了VWF表达。
下调Rictor抑制低剪切应力诱导的血管性血友病因子表达
接下来探讨了Rictor在LSS诱导的VWF表达中的作用。结果显示,下调Rictor抑制LSS诱导的VWF表达。在体外,siRNA用于沉默Rictor,免疫印迹显示下调Rictor抑制LSS诱导的VWF蛋白表达。结果表明,Rictor介导了LSS诱导的VWF表达。
血管内皮钙粘蛋白下调降低了低剪切应力促进的血管性血友病因子表达
为了探索VE-钙粘蛋白对LSS刺激下VWF表达的影响,实验首先使用了免疫印迹(图4 A)和 PCR (图4 B)检测以验证CDH5(VE-钙粘蛋白的基因名称)的三个siRNA序列,并选择具有最佳敲低效果的序列进行后续实验。免疫印迹和IF检测显示,LSS刺激诱导的VWF表达上调依赖于VE-钙粘蛋白(图4 C、D)。这些结果表明,LSS至少部分通过VE-钙粘蛋白调节VWF,并表明Rictor/VE-钙粘蛋白/VWF通路介导LSS诱导的内皮完整性破坏。
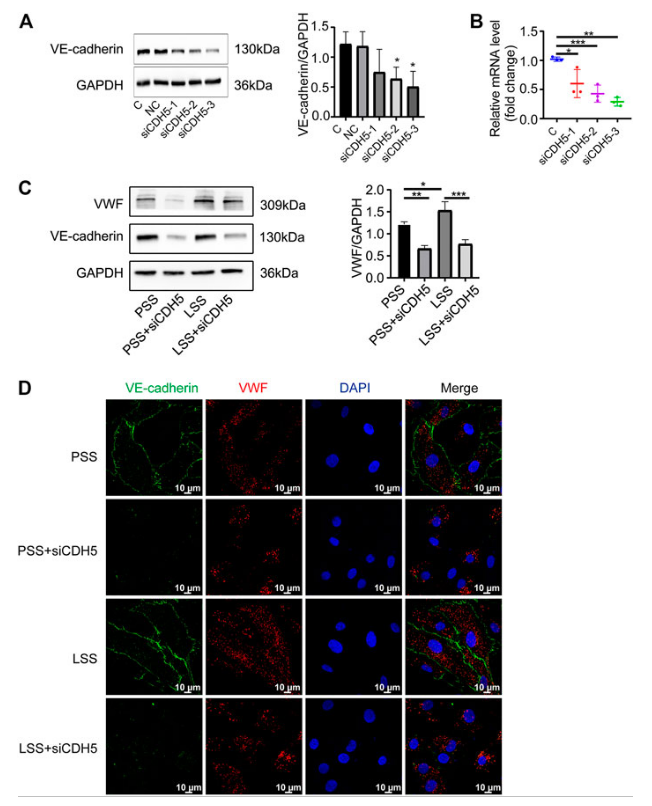
图4 VE-钙粘蛋白的下调降低了VWF表达。
(A)代表性图像显示VE-钙粘蛋白(CDH5)的敲低。C和NC分别代表对照组和阴性对照组。(B)PCR检测CDH5敲低效率。(C)VWF蛋白的表达是在不同类型的剪切应力和有或没有siCDH5 siRNA转染下通过免疫印迹检测的。(D)免疫荧光图像显示VE-钙粘蛋白下调降低了VWF表达。
总之,该研究首次报道了Rictor在LSS下通过调节内皮AJs和VWF在维持血管内皮完整性和介导内皮损伤方面发挥作用。此外,Rictor同时影响PSS和LSS下的AJs和VWF蛋白,表明它可能是一种机械传感器,它的存在在机械转导过程中起着重要作用。
参考文献:Li H, Zhou WY, Liu YX, Xia YY, Xia CL, Pan DR, Li Z, Shi Y, Chen SL, Zhang JX. Rictor maintains endothelial integrity under shear stress. Front Cell Dev Biol. 2022 Nov 10;10:963866. doi: 10.3389/fcell.2022.963866. PMID: 36438564; PMCID: PMC9685313.
原文链接:https://pubmed.ncbi.nlm.nih.gov/36438564/
小编旨在分享、学习、交流生物科学等领域的研究进展。如有侵权或引文不当请联系小编修正。
微信搜索公众号“Naturethink”,了解更多细胞体外仿生培养技术及应用

新鲁汶大学的公报指出,如今抗生素耐药菌的出现给人类和医药带来了新 ...

根据“生物安全关键技术研发”重点专项评审工作安排,生物中心将于2 ...

为更好的向用户、潜在用户提供我们的产品,即日起推出如下活动:凡向 ...

2018年度国家科学技术奖提名工作已结束,国家科学技术奖励工作办 ...

据英国《自然·通讯》杂志日前发表的一篇医学论文报告,科学家发现了 ...

“免疫系统在高血压中扮演了未曾预料的重要角色。”英国格拉斯哥大学 ...

“来一场中国制造的品质革命!”3月5日,李总理在政府工作报告中发 ...

我司自主研发产品,重视知识产权,已拥有多项专利证书! ...

美国侨报网近日刊文称,一项新出炉的研究警告称,即使是失眠一夜,也 ...
公司完成细胞张应变与压力综合培养仪器的研发; ...

Naturethink网站及微信内容逐步完善,敬请查阅! ...

为提高区域自主创新能力,推进区域科技创新体系建设,加大创新驱动区 ...

2018年春节将至,我司放假时间安排为:2月14日至2月21日, ...

澳大利亚和英国一项研究显示,对于几乎任何年龄段的人群而言,快走都 ...

2018年国家自然科学基金项目申请工作已开始,你准备好了吗? ...
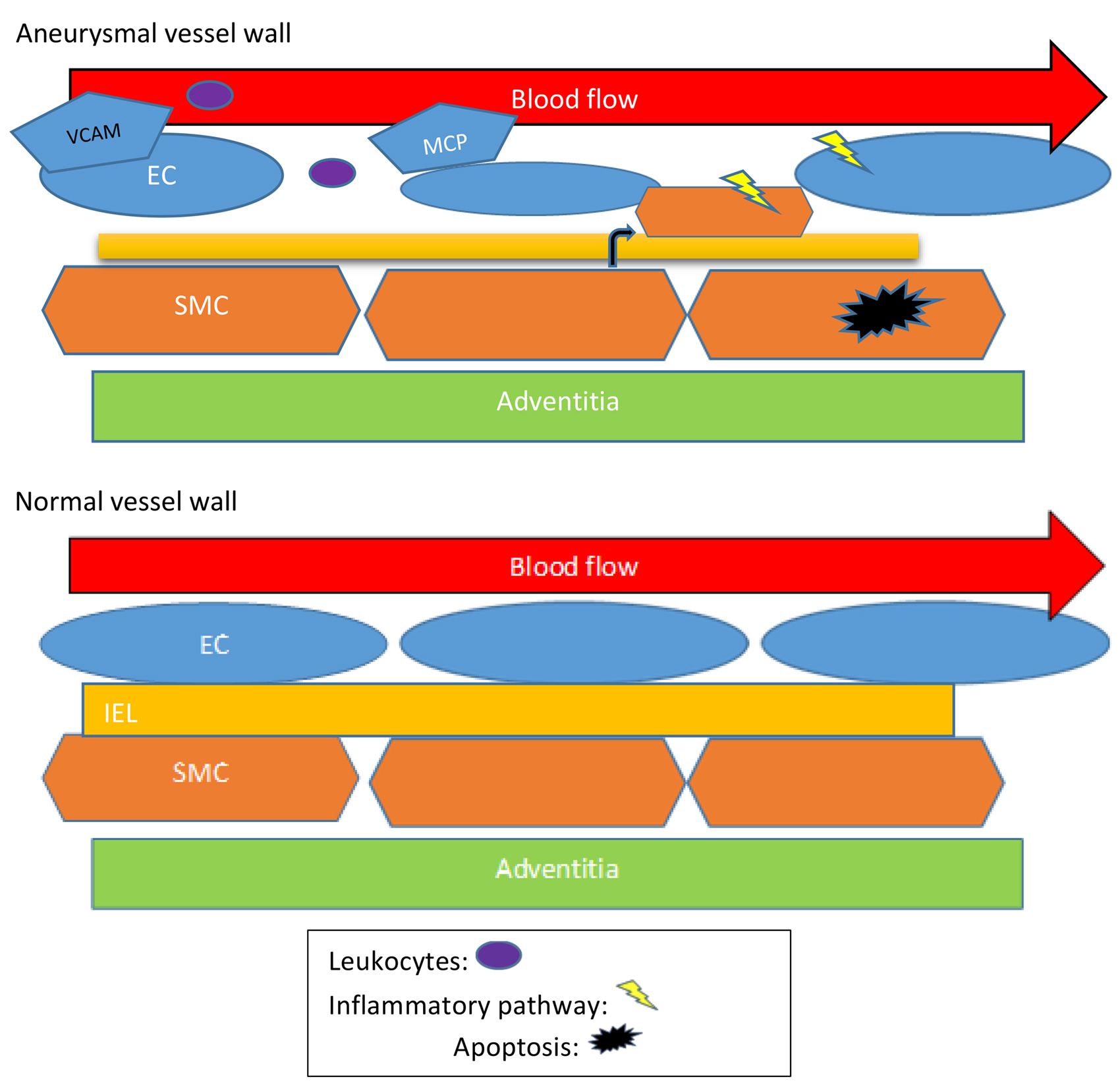
壁面剪切应力(WSS),是单位面积上由血管表面流动的液体产生的接 ...

...
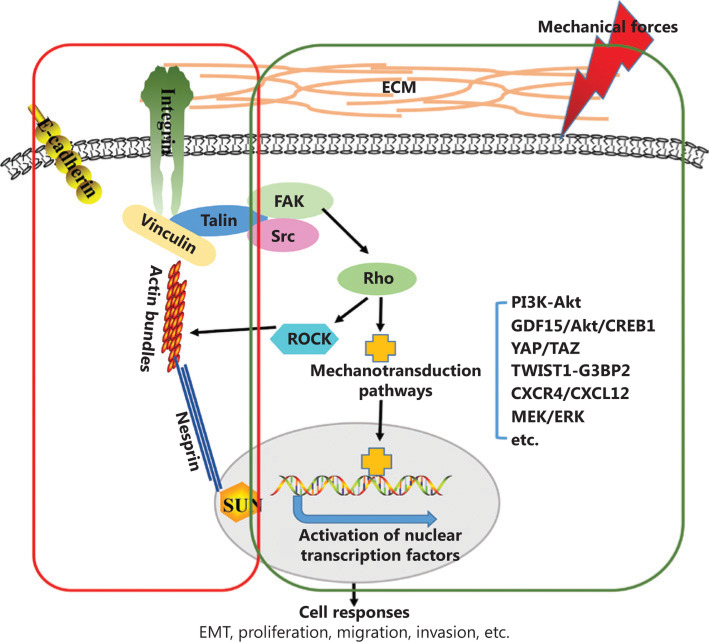
癌症在促进肿瘤表型表观遗传重编程和修饰的复杂组织微环境中发展。此 ...