动脉粥样硬化及其并发症,如冠状动脉疾病、脑血管疾病和外周动脉疾病及其急性并发症,是目前我国发病和死亡的主要原因。已经描述了许多危险因素,传统的危险因素包括吸烟、糖尿病、高胆固醇血症、动脉高血压、肥胖等。然而,血流动力学因素也在斑块的形成或破裂中起重要作用。这些包括切向应力(动脉血压)、脉动心脏输出的周期性拉伸和壁剪切应力(WSS)。在捷克共和国查理大学第一医学院、拉贝河畔乌斯季扬·埃万盖利斯塔·普尔基涅大学的一项研究中,讨论了WSS在动脉粥样硬化发生中的作用,以及WSS评估的可能性。

由于流体流动和两个相邻层具有不同的速度,因此在该界面处会产生剪切应力。剪切应力取决于这些层之间的速度梯度和液体的粘度。同样,流动的液体(血液)和血管壁之间存在速度梯度。为了描述这种相互作用,使用了壁剪切应力(WSS)的概念。WSS 定义为流体在壁面上切向施加的剪切应力。WSS 决定了流体与管壁之间的相互作用程度。对于简化的 WSS 评估,使用以下公式:WSS = (4 μ.v)/r 。其中μ是粘度,v = 速度,r = 动脉半径。
如果我们关注对称性狭窄(例如由于对称性动脉粥样硬化斑块)中的WSS,血流可以分为4个部分:(1)入口,(2)节流或狭窄,(3)血流分离(肩部远端斑块)和(4)出口。(图1)
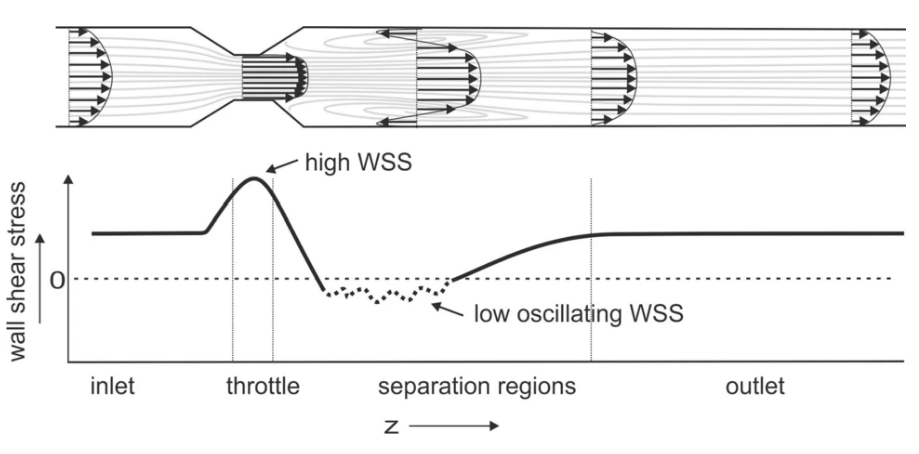
图1 沿对称狭窄的壁面剪切应力示意图。
(1)入口部分,其中流动的性质和剪切应力由边界条件决定。(2)接下来是收缩部分,其中速度曲线由于加速度而变平。在这个区域,速度剖面几乎可以像活塞一样,并且由于壁面附近的速度梯度大,壁上的剪切应力值相对较高。(3)在收缩之外,可以看到加速的平均流,由于粘性力而逐渐减慢,其面积扩大到重新附着在壁上的点。该截面中的壁剪切应力由分离区域的大小和其中流动的性质决定。然而,一般来说,与喉部中的流动相比,剪切应力显著降低,并且反向和不稳定的流动导致应力变为负的和振荡的。(4)在出口部分,剪切应力在流体重新附着后恢复为正值。
在循环中,内皮细胞(ECs)永久暴露于由血流引起的WSS。血流的局部模式决定了WSS的特征,即其强度、方向、脉动性和规律性,这些特征由内皮细胞感知。EC对WSS的敏感性涉及血管发育和生理过程,例如发育血管形成过程中的血管结构模式、血管反应性和血管重塑。WSS 影响内皮细胞的形态、内膜增殖、分化、代谢和通讯。在健康条件下,内皮代谢活性高,有丝分裂稳定。
在没有严重动脉粥样硬化危险因素的健康儿童中,动脉相对笔直,动脉壁薄,内皮层功能完整,分叉往往具有与最小能量损失相关的锐角。与衰老相关的动脉壁结构改变包括组织学改变(弹性蛋白减少、胶原蛋白增加、动脉粥样硬化和内侧钙质沉着)以及动脉扩张和延长。随着年龄的增长和各种疾病,动脉不仅扩张而且拉长。只要成年人体不生长,动脉就没有伸长的空间。因此,各种拱形、弯曲、扭结或卷曲发展,分叉角度变得更加像钝角。这些变化导致相当大的血流改变(湍流而不是层流),从而导致了易发生动脉粥样硬化的WSS紊乱。
研究表明,可能有数十种蛋白质和细胞结构参与感知和机械传递(将机械力转化为生化过程和信号通路的过程),而不是一个特定的分子作为WSS受体。
目前提出了几种分子来发挥机械转导的功能:初级纤毛、整合素、糖萼和离子通道。例如,内皮细胞连接复合物中的一种蛋白质称为PECAM-1(血小板内皮细胞粘附分子-1)一直是多项研究的主题。PECAM-1张力增加会触发激酶,并通过磷酸化激活血管内皮生长因子受体,后者在血管生成中起重要作用。另一种可能的WSS感知方法已被推广,它基于张拉整体的原理。这种观点关注细胞的微结构,主要是细胞骨架,是主要的传感器。通过张力,人们可以看到细胞的形状是作用在不同方向的拉力之间精细平衡的净结果。当有力从外部推动时,细胞骨架会感应到变形,并触发生化过程。
在直动脉段中,血流呈层流状,WSS 值在生理上保持在 10–50 dyne/cm2 的狭窄范围内。当血流需求增加时,例如在步行、慢跑等过程中,下肢的外周动脉阻力(小动脉张力)降低,而流速和容量增加。速度的提高意味着更高的 WSS。这被ECs检测到,并释放更多的一氧化氮以扩大供血动脉的直径,并使WSS正常化。然而,这种理想的机制在具有相对固定几何形状的动脉段中是无法实现的,例如在分叉的外壁(图2)或沿主动脉弓的内壁,其中血流比沿外壁慢。事实上,这些部位最常受到动脉粥样硬化的影响。内皮细胞倾向于与壁剪切应力对齐:壁剪切应力越高,细胞越细长,反之亦然。在狭窄的动脉段中,内皮细胞在分离区失去其细长的形状(图1)。颈内动脉最近端具有高度神经支配的扩张,称为颈动脉窦,也是斑块的常见部位。在颈动脉窦中,动脉内径突然变宽,无法流动,出现所谓的流动逆转模式,并可通过双多普勒超声显示(图2),甚至可以定量。
然而,与健康对照组相比,直动脉段的WSS在各种疾病状态(如2型糖尿病和终末期肾病)中也长期较低。更重要的是,较低的颈总动脉WSS与较高的内膜-中膜厚度、更多的颈动脉分叉斑块有关,但也与老年受试者的脑白质高信号和认知障碍有关。同样,低振荡WSS区域首先受到冠状动脉壁增厚的影响。
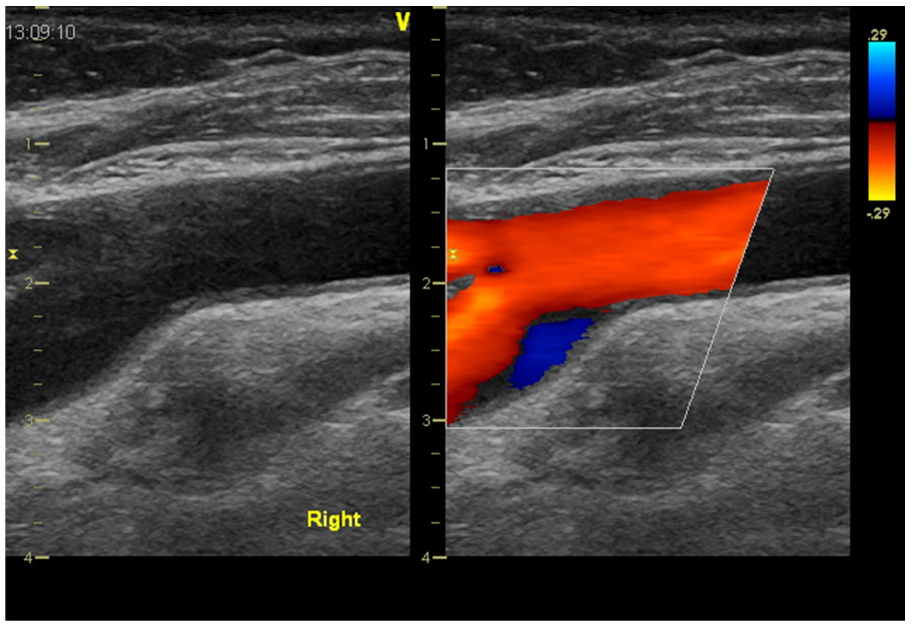
图2 颈动脉分叉时血流逆转。
颈动脉分叉纵切面在B模式(左)和彩色多普勒图(右)的图像。颈内动脉从扩张的部分(球状或窦)开始。在收缩期,直线段的血流加速,但在颈动脉窦(蓝色区域)发生血流逆转。颈动脉窦中的低振荡WSS是动脉粥样硬化斑块早期发展的原因。
WSS高的区域包括动脉狭窄(图1),严重主动脉瓣狭窄时的升主动脉,以及动静脉瘘或畸形的供血动脉。在狭窄段中,狭窄部分之后是流动分离区域,其中WSS变低并具有振荡矢量。
长期高WSS的影响既是机械的,也是生化的。机械作用包括内皮细胞剥蚀、纤维帽变薄、斑块出血和钙化,但当斑块不是圆形时,还包括管腔扩张。对体液的影响包括增加一氧化氮的产生,但也包括生长因子的产生和血管性血友病因子的激活等。换句话说,长期较高的WSS会导致斑块不稳定和破裂。
WSS变化与危险因素一起在动脉粥样硬化的发展中起着关键作用。具有长期低WSS的动脉部位由于其几何形状和管壁变化而无法通过直径缩小做出反应,首先受到斑块的影响。这是由于内皮通透性和功能发生了变化。然而,已经表明,一些患者在直动脉段(特别是在颈总动脉)中也有较低的WSS。原因可能是年龄和疾病介导的动脉扩张。颈总动脉中较低的 WSS 可预测存在分叉斑块和脑白质高信号的存在。高 WSS 发生在动脉狭窄中,似乎会导致斑块不稳定和凝血激活。
参考文献:J M, L N, A V, E C, V L, K BS, L L, T G, M P, P M. Wall Shear Stress Alteration: a Local Risk Factor of Atherosclerosis. Curr Atheroscler Rep. 2022 Mar;24(3):143-151. doi: 10.1007/s11883-022-00993-0. Epub 2022 Jan 26. PMID: 35080718.
原文链接:https://pubmed.ncbi.nlm.nih.gov/35080718/
小编旨在分享、学习、交流生物科学等领域的研究进展。如有侵权或引文不当请联系小编修正。
微信搜索公众号“Naturethink”,了解更多细胞体外仿生培养技术及应用

新鲁汶大学的公报指出,如今抗生素耐药菌的出现给人类和医药带来了新 ...

根据“生物安全关键技术研发”重点专项评审工作安排,生物中心将于2 ...

为更好的向用户、潜在用户提供我们的产品,即日起推出如下活动:凡向 ...

2018年度国家科学技术奖提名工作已结束,国家科学技术奖励工作办 ...

据英国《自然·通讯》杂志日前发表的一篇医学论文报告,科学家发现了 ...

“免疫系统在高血压中扮演了未曾预料的重要角色。”英国格拉斯哥大学 ...

“来一场中国制造的品质革命!”3月5日,李总理在政府工作报告中发 ...

我司自主研发产品,重视知识产权,已拥有多项专利证书! ...

美国侨报网近日刊文称,一项新出炉的研究警告称,即使是失眠一夜,也 ...
公司完成细胞张应变与压力综合培养仪器的研发; ...

Naturethink网站及微信内容逐步完善,敬请查阅! ...

为提高区域自主创新能力,推进区域科技创新体系建设,加大创新驱动区 ...

2018年春节将至,我司放假时间安排为:2月14日至2月21日, ...

澳大利亚和英国一项研究显示,对于几乎任何年龄段的人群而言,快走都 ...

2018年国家自然科学基金项目申请工作已开始,你准备好了吗? ...
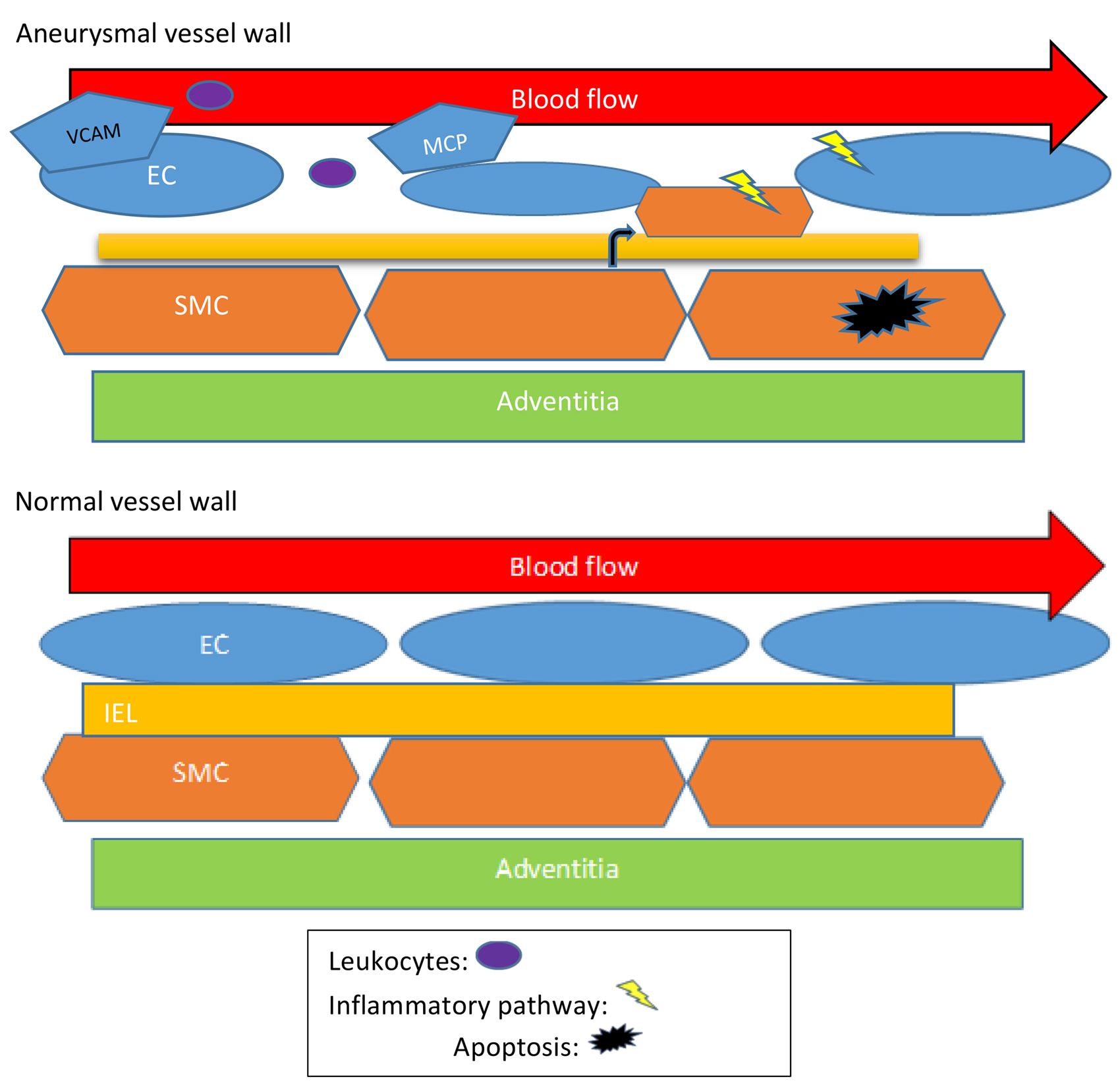
壁面剪切应力(WSS),是单位面积上由血管表面流动的液体产生的接 ...

...
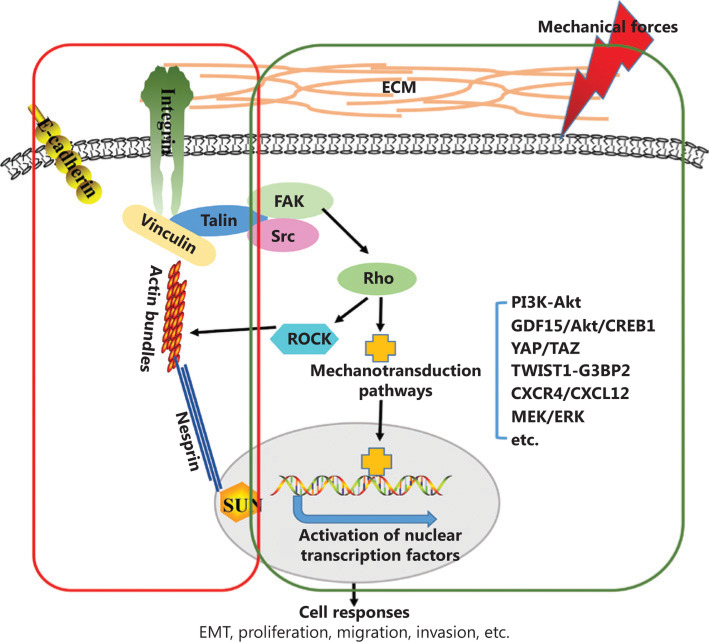
癌症在促进肿瘤表型表观遗传重编程和修饰的复杂组织微环境中发展。此 ...