慢性肾衰竭折磨着全球200多万患者。目前的治疗选择是透析和器官移植。虽然肾移植提供了最佳的临床结果,但供体器官的严重短缺往往迫使肾脏患者长时间接受透析,导致生活质量差和死亡率增加。因此,拥有一个小巧、便携式的,可批量生产并最终可植入的“生物人工肾”将是非常有益的,它可以执行最关键的肾脏功能。
目前开发的方法包括基于细胞的策略,其目的是创建一个功能齐全的替代器官;以及基于透析技术的可穿戴式人工肾脏装置,允许患者在临床环境之外接受长期和频繁的治疗;和试图模仿天然肾单位的关键功能的生物混合设备。
美国加州大学旧金山分校生物工程与治疗科学系的研究团队在利用生物混合方法开发一种可植入的生物人工肾脏,可以执行最关键的肾脏功能并减轻患者透析的负担,相关研究成果发表在 Journal of Microelectromechanical Systems 题为《A Scalable, Hierarchical Rib Design for Larger-Area, Higher-Porosity Nanoporous Membranes for the Implantable Bio-Artificial Kidney》。该项目研发的生物装置利用纳米多孔硅膜作为构建生物兼容性血液过滤器和肾小管细胞生物反应器的基本基础技术,它们将协同工作以选择性地分离血液废物并重新吸收盐和水(图1)。这项重大进展可以说是临床前研究的一个重要里程碑。

图1 植入式生物人工肾概念。一部分是血液过滤器,可以通过使血液透过精确形状的纳米级孔的硅膜来去除血液中的毒素,另一个部分是包含人工培养的人肾小管细胞的生物反应器,旨在实现除血液滤过以外的其他肾功能,比如,维持体液水和电解质平衡,维持血压,以及代谢功能,并产生必需的激素。其中,纳米多孔硅膜为血液过滤器和生物反应器提供了基本的赋能技术。
在膜的设计层面,直接影响传质效率的一个明显因素是活性膜面积与整体芯片面积的比值。在当前的“Gen 1”(第一代)器件中,大约40% 的芯片面积是深反应离子刻蚀(DRIE)bulk-Si “框架”(图2 左)所占用的死区,其中框架是起始基板的全部厚度。因此,该团队提出了一种“Gen 2” (第二代)设计,其脚手架更薄,更轻(图2 右),为有源滤波器留出更多空间。
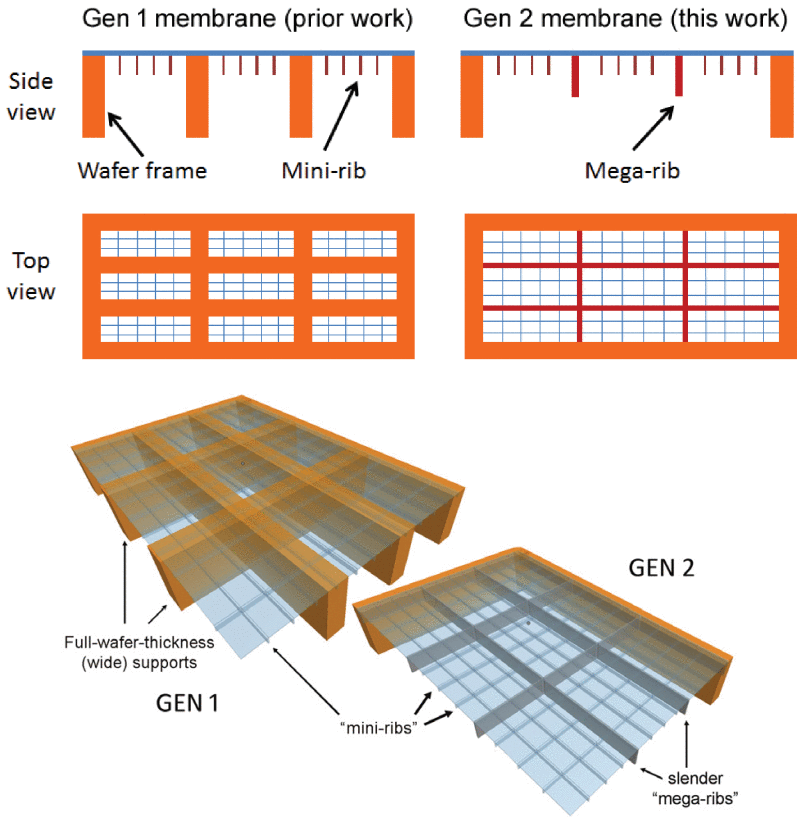
图2 第1代和第2代肋状膜的比较。在第2代中,许多全晶圆厚度的支撑物(橙色)被多晶硅膜下更细长的“巨型肋骨”所取代,从而释放了更多的过滤面积。
在这项工作中,研究人员专注于用多晶硅“mega-ribs”取代大多数40 μm-宽,40 μm-高的DRIE定义的高“walls”,相比之下,多晶硅窄4倍,浅10倍(图2 右),旨在将多孔区域填充因子从 63% 提高到 88%(即增益40%)。
此外,在实验过程中,研究人员还注意到以下两种因素的影响。
A. 流体考虑因素
这些较浅的“mega-ribs” 的采用也部分受到流体动力学的驱动。在目前的生物人工肾脏设计中,血液平行于顶部膜表面流动,滤液沿底部膜表面逆平行流动。然而,由于晶圆框架的厚度,大多数活性滤液流动实际上发生在距离膜平面相当远的距离(数百个μm),减慢了毒素的去除速度,从而阻碍跨膜扩散。因此,进行了计算流体动力学(CFD)建模,以研究是否值得使背面支撑结构缩短或简化。
出于仿真的目的,使用ANSYS Fluent 19.2软件(图3)。分析表明,大幅降低滤液侧400 μm高的“障碍物”的高度将使分子通过膜的质量运输提高近4倍。换句话说,将“mega-ribs” 整合到支撑结构中肯定有助于提高过滤效率。
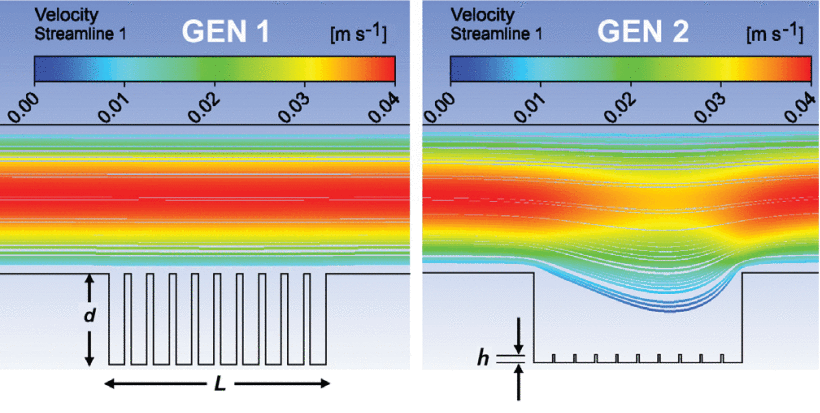
图3 计算流体动力学(CFD)模拟流体流动(从左到右)经过(i)紧密间隔的数组400 μm-高晶圆厚支架 (Gen 1 左)和(ii)较短(h=40μm)的mega-ribs(第2代 右)。在Gen 2中,流体流浸入蚀刻腔,从而促进毒素的去除。仿真结果表明,其质量传输系数可提高近4倍。
B. 机械考虑因素
除了微流体性能外,还关注mega-rib 膜设计的机械力学特性。在之前的工作中,标准的膜“窗口”是100×400μm,但现在正试图使用 mega-ribs 将其扩展到 1000×4000μm (即面积大100倍)使用巨型肋骨。这样做,必须确保如此大的独立式跨度在机械上仍然是合理的,即膜刚度不会因收缩支撑而过度受损。
因此,转向有限元分析(FEA)来比较旧设计与新设计。该研究的所有机械建模均使用了ANSYS机械19.2软件,并对膜的血液接触表面施加300 mmHg的压力。图4 显示了简单的 FEA 结果,100×400μm (non-ribbed)膜与1000×4000μm (mega-ribbed)膜在恒定的分布式载荷下,结果表明 mega-rib 膜刚度虽然高出5倍,但仍然可以接受。

图4 有限元分析(FEA)结果显示,各种尺寸(0.6×4 mm、0.8×4 mm、1.0×4 mm)的 Gen 2 mega-rib 膜的最大挠度(“m.d.”)。为了加快模拟速度,使用了四分之一膜模型来利用设计的对称性。右下角的小单元代表旧的Gen 1(non-ribbed)设计。
为了扩展经过验证的基于肋的设计,研究开发了一种可扩展的、分层的基于肋的MEMS制造方法,可实现具有明显更高孔隙率和质量传递系数的大跨度、高填充系数的纳米多孔膜。从制造的角度来看,这种方法有望降低制造成本,同时保持制造产量。从设计的角度来看,它通过提供多个可以独立调整的设计参数来优化孔隙率和鲁棒性之间的平衡,从而增加了灵活性。总之,随着mega-rib 设计的引入以及其他工艺改进(例如更高分辨率的步进光刻术以增加孔密度),生物人工肾脏的芯片吞吐量和整体性能的提高是指日可待的。
参考文献:Chui B W , Wright N J , Ly J , et al. A Scalable, Hierarchical Rib Design for Larger-Area, Higher-Porosity Nanoporous Membranes for the Implantable Bio-Artificial Kidney[J]. Journal of Microelectromechanical Systems, 2020, PP(99):1-7.
DOI:10.1109/JMEMS.2020.3013606
小编旨在分享、学习、交流生物科学等领域的研究进展。如有侵权或引文不当请联系小编修正。
微信搜索公众号“Naturethink”,了解更多细胞体外仿生培养技术及应用!

新鲁汶大学的公报指出,如今抗生素耐药菌的出现给人类和医药带来了新 ...

根据“生物安全关键技术研发”重点专项评审工作安排,生物中心将于2 ...

为更好的向用户、潜在用户提供我们的产品,即日起推出如下活动:凡向 ...

2018年度国家科学技术奖提名工作已结束,国家科学技术奖励工作办 ...

据英国《自然·通讯》杂志日前发表的一篇医学论文报告,科学家发现了 ...

“免疫系统在高血压中扮演了未曾预料的重要角色。”英国格拉斯哥大学 ...

“来一场中国制造的品质革命!”3月5日,李总理在政府工作报告中发 ...

我司自主研发产品,重视知识产权,已拥有多项专利证书! ...

美国侨报网近日刊文称,一项新出炉的研究警告称,即使是失眠一夜,也 ...
公司完成细胞张应变与压力综合培养仪器的研发; ...

Naturethink网站及微信内容逐步完善,敬请查阅! ...

为提高区域自主创新能力,推进区域科技创新体系建设,加大创新驱动区 ...

2018年春节将至,我司放假时间安排为:2月14日至2月21日, ...

澳大利亚和英国一项研究显示,对于几乎任何年龄段的人群而言,快走都 ...

2018年国家自然科学基金项目申请工作已开始,你准备好了吗? ...
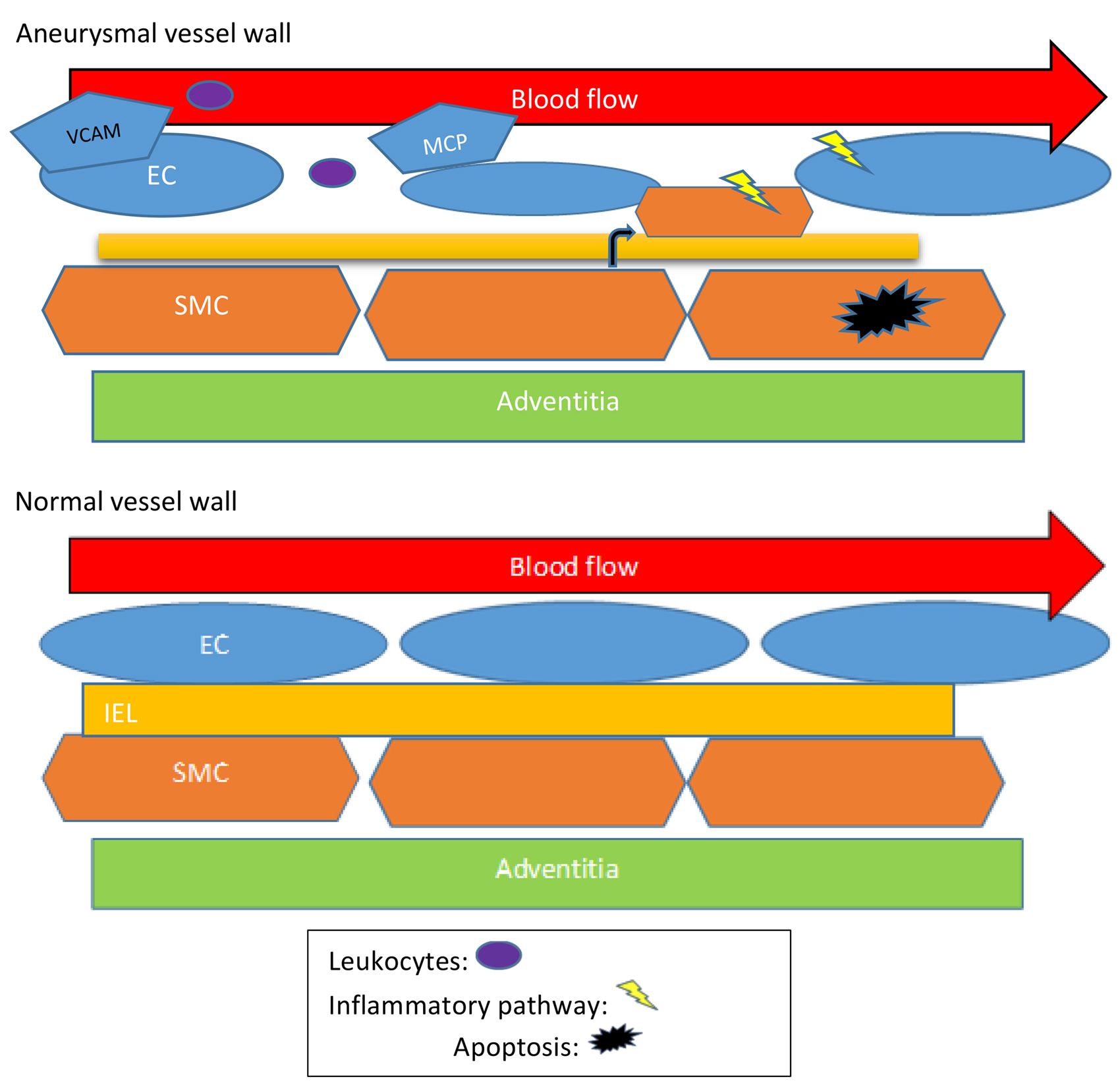
壁面剪切应力(WSS),是单位面积上由血管表面流动的液体产生的接 ...

...
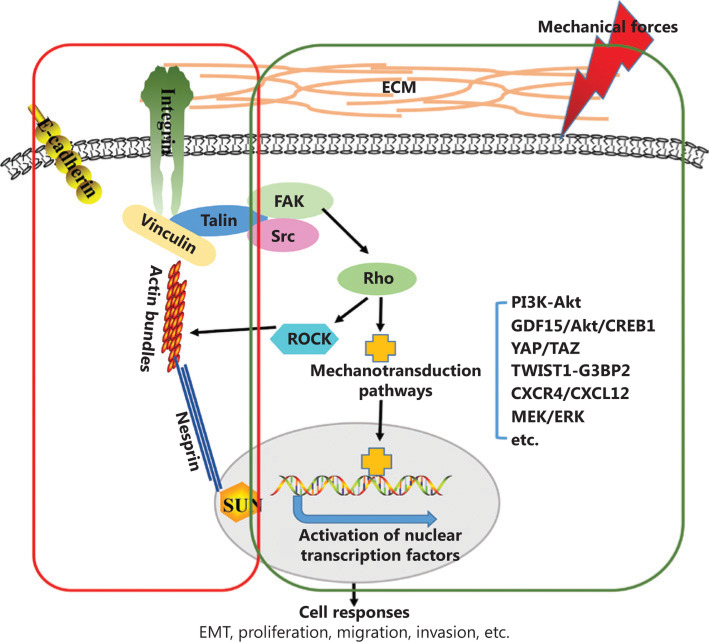
癌症在促进肿瘤表型表观遗传重编程和修饰的复杂组织微环境中发展。此 ...