心脏瓣膜的发育始于内皮-间充质转化(EMT),其中瓣膜内皮细胞(VEC)获得间充质标志物并侵入内皮下基质形成心脏内膜垫。EMT后,这些细胞增殖并分化成细胞外基质(ECM),产生瓣膜间质细胞(VIC)。通过VEC和VIC的精确调控,完全舒张的心内膜垫经过ECM重塑并拉长成细长的瓣叶。在此过程中,生长和重塑受到干扰会导致瓣膜畸形,从而导致临床上相关的心脏缺陷。这种干扰的遗传原因已经被广泛研究,但只能解释不到 20% 的临床病例。机械应力在调节瓣膜发育中的重要性已得到广泛认可。振荡剪切应力 (OSS)促进 EMT,其细胞和分子机制已得到充分了解。相比之下,机械力在临床上重要的EMT之后的生长和重塑中的作用仍然知之甚少。
流动的血液在瓣膜上产生剪切和静水应力。剪切应力与 VECs 直接接触,而静水应力在瓣膜中引起压缩力和拉伸力,并可传递到 VICs。已在成人组织中鉴定出多种机械敏感信号通路,但它们与瓣膜形态发生的关系尚不清楚。YAP信号是另一种被广泛研究的机械活性通路,是Hippo 通路的转录辅因子。已知YAP信号通过促进心肌细胞增殖来调节心室发育。然而,它在 EndMT 后瓣膜形态发生中的作用知之甚少。此外,YAP通路是否对不同细胞类型的不同应力做出不同的反应,以及这些机械反应如何协同调节多种细胞类型以实现特定的组织形态发生,尚不清楚。
最近,美国康奈尔大学梅尼格生物医学工程学院研究组在《eLife》发表了题为“Shear and hydrostatic stress regulate fetal heart valve remodeling through YAP-mediated mechanotransduction”的文章,探讨了剪切和静水应力调控瓣膜生长和重塑的机制。该团队使用体外和离体模型来解耦剪切和静水应力对瓣膜尺寸和形状的影响,还研究了YAP介导的机械转导在这些效应中的作用。通过结合这些模型,详细阐述了剪切和静水应力如何调节VEC和VIC,以确定瓣膜的合适尺寸和形状。

YAP表达受时空调控
实验首先收集了野生型小鼠不同发育阶段的胚胎心脏,并检查了心脏瓣膜中的YAP激活情况。结果发现,在E11.5(胚胎期)时,YAP在流出道(OFT)和房室(AV)缓冲层的间质和内皮中均有表达。在E14.5时,VIC中YAP激活显著升高,然后在E17.5时下降。在后期重塑阶段,YAP激活的这种降低在房室瓣膜中是显著的,但在左室瓣膜中不明显,因为所有瓣膜的发育并不均匀。在流出侧的VECs中,细胞核YAP表达在后期重塑阶段显著增加。尽管在流入侧的VECs中,细胞质YAP表达在所有阶段都更强。
此外,还在汉堡-汉密尔顿(Hamburger–Hamilton stages)阶段(HH)25、HH30和HH36检测了鸡胚胎心脏中YAP的活性,它遵循相同的时空模式。VICs中的YAP激活在HH30激增,然后在HH36下降。流出侧的VECs具有上调的核YAP表达,而流入侧VECs的YAP表达主要在细胞质中。
进一步检测YAP转录活性,以确定YAP激活的上游。与E11.5或HH25缓冲层相比,YAP靶基因THBS1,ANKRD1和PTX3在E14.5和HH31处分别升高了近10倍。这些基因的表达随后在重塑的后期阶段显著降低。相比之下,LATS1/2(Hippo 通路中YAP的上游)的基因表达在瓣膜生长和重塑过程中几乎没有变化。这表明YAP活性在很大程度上独立于Hippo 通路。
剪切和静水应力调节YAP活性
除了Hippo 通路的协同效应外,YAP也是机械转导的关键介质。事实上,YAP的时空激活与机械环境的变化相关。在瓣膜重塑过程中,单向剪切应力(USS)在瓣膜的流入表面上产生,其中YAP很少在VECs的核中表达(图1 A)。另一方面,振荡剪切应力(OSS)在流出表面上发生,其中核YAP定位在VECs。VICs中的YAP激活也与静水应力相关。应力在瓣膜尖端产生压应力(CS),其中核 YAP 定位在 VICs(图1 B)。尽管拉伸应力(TS)是在伸长区域产生的,但YAP在VIC核中不存在。
为了研究剪切应力对VECs中YAP活性的影响,实验将USS和OSS直接应用于VECs,发现低OSS(2 dyn/cm2)促进 VEC 中的 YAP 核易位(图1 C、E),而高USS (20 dyn/cm2)抑制了细胞质中的YAP。
为了研究静水应力对VICs中YAP活化的影响,实验使用具有不同渗透压的培养基来模拟CS和TS。在不同负荷条件下培养HH27 AV缓冲层外植体24 h,发现梯形缓冲层呈球形(图1 D)。TS加载后缓冲层显著压缩,VICs中YAP活化显著低于CS加载的VICs(图1 F)。

图1 剪切应力和静水应力调节YAP活性。
YAP的缺失限制了细胞增殖并促进瓣膜成形
为了研究YAP在瓣膜生长和重塑中的功能,在CS(促生长)和U(卸载)条件下添加了YAP的药理学抑制剂维替泊芬(VP)。抑制YAP减小了缓冲层的大小。与在CS下培养的缓冲层的球形状相反,在具有VP的培养基中培养的瓣膜保持其梯形形状。进一步的研究表明,YAP的缺失显著抑制了VIC的增殖。此外,YAP抑制显著增强了VECs之间VE-钙粘蛋白的表达。缓冲层通常只有一层内皮,但YAP抑制的瓣膜显示五层或更多层内皮。
激活YAP促进细胞增殖并抑制瓣膜伸长
为了研究YAP的功能获得性,在TS(促压缩)和U条件下添加一个YAP 转录活性的特异激活剂PY-60。YAP激活扭转了瓣膜在TS和U条件下的压缩趋势,并推动了瓣膜尺寸的增长(图2 A、B)。所有瓣膜都呈球形,无论它们是生长还是被压缩。pHH3染色显示,无论加载条件如何,YAP活化显著提高了VIC增殖(图2 C、G)。VE-钙粘蛋白在YAP活化的内皮中的表达明显弱于YAP被抑制的内皮(图2 D)。
图2 激活YAP可促进细胞增殖,抑制瓣膜伸长。
抑制YAP促进体内样刚度增加
为了评估YAP在瓣膜刚度中的作用,实验测量了VP或PY-60处理的缓冲层外植体的应变能量密度。这种方法已被应用测量不同发育阶段雏鸡胚胎瓣膜的机械性能。结果表明,从HH25到HH34,瓣膜刚度几乎呈线性增长,几乎每24小时翻一番。在这项研究中发现,抑制YAP在24小时培养期间也给出了类似的硬度增加(图2 H)。尽管YAP激活和抑制都增加了瓣膜刚度,但激活YAP后瓣膜的刚度仅为抑制YAP时的一半。
体内机械操作导致瓣膜缺损和YAP失调
为了操纵体内的机械力,实验在AV缓冲层生长的早期阶段(HH24)进行了左心房结扎(LAL)。LAL限制了左心室的血流,导致左室瓣膜的血流动力学应力和剪切应力降低,但右室瓣膜的力增加。结果,LAL瓣膜和心脏(图3 A)的尺寸小于对照瓣膜和心脏(图3 B)。具体而言,LAL导致左房室间隔瓣发育不全且呈球形,而右房室间隔瓣过度发育和拉长。这与正常的瓣膜发育相反,在正常瓣膜发育期间,左房室瓣膜的尺寸要大得多,并且更细长(图3 C)。对照组中YAP激活在左右AV中均较高,而LAL导致不平衡的YAP激活:右室AV YAP激活高,而左室AV激活显著降低(图3 D)。

图3 中断的生物力学改变了YAP的激活并导致体内瓣膜缺损。
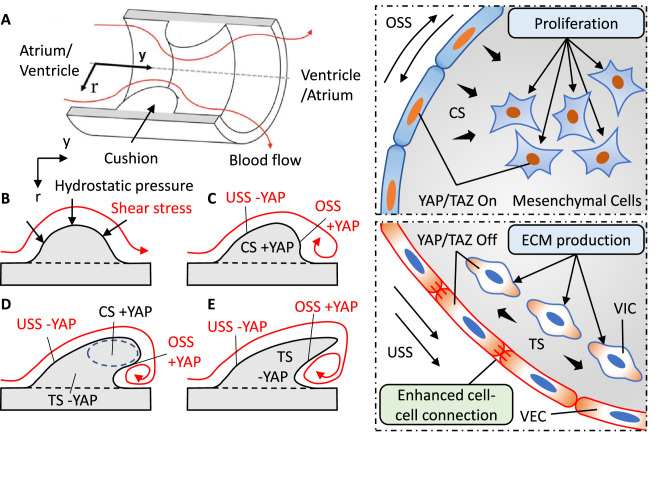
图4 剪切应力和静水应力的局部协作可以通过YAP信号引导复杂的形态发生。
(A)房室管或 OFT 中对称心内膜垫的模型。(B)模型的横截面显示流动的血液在缓冲层上产生静水应力和剪切应力。(C)振荡剪切应力(OSS)和压应力(CS)分别促进了VEC和VIC的YAP核易位。单向剪切应力(USS)抑制了YAP核易位。CS通过刺激间充质细胞的增殖来促进缓冲层生长。(D)剪切应力通过调节VECs之间的细胞-细胞粘附来驱动缓冲层重塑为小叶结构。(E)拉伸应力(TS)抑制YAP核易位与USS共同作用,形成紧凑而细长的形态。
总之,该研究表明,剪切应力和静水应力的时空协调机械转导是瓣膜生长和重塑所必需的。剪切应力和静水应力可以通过YAP通路调节VEC张力和VIC增殖,从而决定瓣膜的尺寸和形状。功能失调的YAP信号可能导致瓣膜畸形,但不正确的局部机械信号传导会带来更重要的畸形风险,即使YAP信号功能齐全且没有基因突变。其中所提出的机械生物学系统还可以通过影响力或在特定阶段靶向YAP通路来控制瓣膜生长和改变瓣膜形状。
参考文献:Wang M, Lin BY, Sun S, Dai C, Long F, Butcher JT. Shear and hydrostatic stress regulate fetal heart valve remodeling through YAP-mediated mechanotransduction. Elife. 2023 Apr 20;12:e83209. doi: 10.7554/eLife.83209. PMID: 37078699; PMCID: PMC10162797.
原文链接:https://pubmed.ncbi.nlm.nih.gov/37078699/
小编旨在分享、学习、交流生物科学等域的研究进展。如有侵权或引文不当请联系小编修正。
微信搜索公众号“Naturethink”,了解更多细胞体外仿生培养技术及应用。

新鲁汶大学的公报指出,如今抗生素耐药菌的出现给人类和医药带来了新 ...

根据“生物安全关键技术研发”重点专项评审工作安排,生物中心将于2 ...

为更好的向用户、潜在用户提供我们的产品,即日起推出如下活动:凡向 ...

2018年度国家科学技术奖提名工作已结束,国家科学技术奖励工作办 ...

据英国《自然·通讯》杂志日前发表的一篇医学论文报告,科学家发现了 ...

Naturethink祝愿伟大祖国繁荣昌盛,欣欣向荣! ...

“免疫系统在高血压中扮演了未曾预料的重要角色。”英国格拉斯哥大学 ...

“来一场中国制造的品质革命!”3月5日,李克强总理在政府工作报告 ...

我司自主研发产品,重视知识产权,已拥有多项专利证书! ...

美国侨报网近日刊文称,一项新出炉的研究警告称,即使是失眠一夜,也 ...
公司完成细胞张应变与压力综合培养仪器的研发; ...

Naturethink网站及微信内容逐步完善,敬请查阅! ...

为提高区域自主创新能力,推进区域科技创新体系建设,加大创新驱动区 ...

2018年春节将至,我司放假时间安排为:2月14日至2月21日, ...

澳大利亚和英国一项研究显示,对于几乎任何年龄段的人群而言,快走都 ...

2018年国家自然科学基金项目申请工作已开始,你准备好了吗? ...
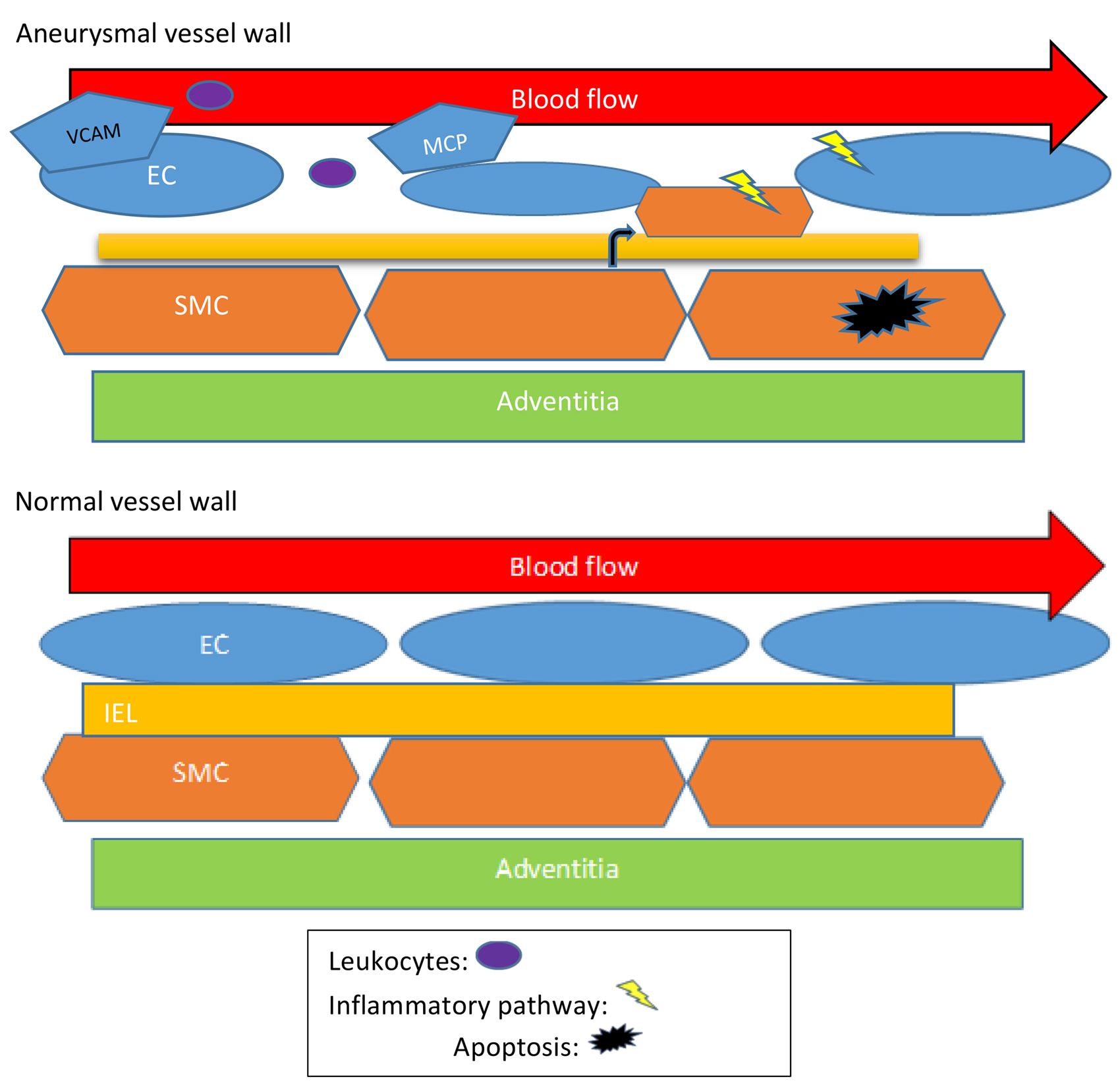
壁面剪切应力(WSS),是单位面积上由血管表面流动的液体产生的接 ...
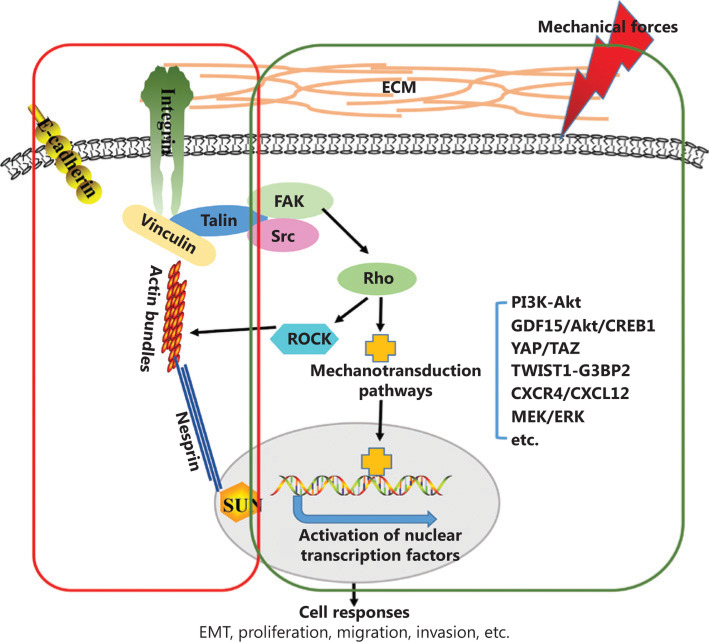
癌症在促进肿瘤表型表观遗传重编程和修饰的复杂组织微环境中发展。此 ...