由机械力触发的正畸牙齿移动 (OTM) 取决于牙根周围组织的重塑。长期以来,人们一直希望加速 OTM 过程,因为它有多种潜在的好处,包括缩短治疗时间和减少副作用。牙周膜细胞 (PDLCs) 是牙周组织中主要的细胞成分之一,负责 OTM 期间的信号转导。到目前为止,PDLCs 中机械应力诱导的遗传变化和机械转导机制仍未完全了解。
巨噬细胞起源于髓系前体,在 M-CSF 和 RANKL 的刺激下可分化为破骨细胞,从而在破骨细胞活性形成和骨吸收过程中发挥关键作用。巨噬细胞可以极化为 M1 和 M2 表型。最近的研究报道了 OTM 期间巨噬细胞M1/M2极化率升高,表明巨噬细胞极化对骨重塑的重要作用。然而,促使力诱导 M1 样极化的因素尚未阐明,这促使我们探索更多力诱导的遗传变化,这会导致巨噬细胞和 PDLCs 在机械转导过程中的功能改变。
生长分化因子15 (GDF15) 是人类转化生长因子β (TGF-β) 超家族的成员之一。与其他家族成员一样,它参与许多信号通路的调控,包括 ERK 和 SMADs 。至于 GDF15 在破骨细胞分化中的作用,已证明缺氧能够诱导 GDF15 表达,促进 NF-κB 活化,从而促进破骨细胞生成。在肿瘤进展中也报道了其对破骨细胞分化的促进作用。
尽管 GDF15 在破骨细胞生成中起关键作用,但很少有研究报道它对机械刺激,特别是压力刺激和随后的生物学事件的反应。基于此,由北京大学口腔医学院、口腔数字医学北京市重点实验室、口腔数字化医疗技术和材料国家工程实验室的专家学者进行了合作研究,旨在探索 GDF15 在人 PDLCs 中对压力的响应及其对破骨细胞分化和巨噬细胞 M1/M2 极化的影响,并进一步剖析了 GDF15 促进破骨细胞生成的可能分子机制,以及施加力后导致 GDF15 上调的上游调控因子。

实验结果:
压力诱导人 PDLCs 中 GDF15 的激活
为了剖析 GDF15 在 PDLCs 机械转导中的作用,首先评估了 GDF15 对压力的响应。为此,将 PDLCs置于0 ~ 1.5 g/cm2的连续压力下持续24 h,然后进行western blot和RT-qPCR检测GDF15的表达变化。
结果表明,在压力刺激下,GDF15 在蛋白质和 mRNA 水平上均显著增加。为了进一步巩固这一点,将 PDLCs 在1.5 g/cm2的压力下持续0 - 24小时。RT-qPCR 的结果也一致证明了 GDF15 表达的上调。因此,这些数据表明 GDF15 在人 PDLCs 中被压力转录上调。
GDF15促进RAW264.7细胞破骨细胞的分化
接下来,实验试图研究GDF15在力刺激下的功能作用,假设 PDLCs 分泌的 GDF15 可能有助于单核细胞的破骨细胞分化。为了测试这一点,在存在或不存在重组 GDF15 蛋白 (rGDF15) 的情况下,在 RANKL 诱导的 RAW264.7 细胞中进行了 TRAP 染色。数据表明,GDF15正调控破骨细胞的分化。
为了探索 GDF15 是否在力诱导的破骨细胞分化中发挥作用,收集GDF15敲低或对照细胞压力处理后的PDLCs上清液,然后将 RAW264.7 细胞与这些上清液共培养。RT-qPCR 的结果显示,CK 和 TRAP 的表达在 GDF15 敲低的细胞中均显著下调,表明 GDF15 在由压力触发的破骨细胞分化中起重要作用。
GDF15 对于力诱导的促炎细胞因子和 RANKL/OPG 比率的上调起重要作用
在确定了 GDF15 对破骨细胞分化的促进作用后,研究人员开始解开其潜在的分子机制。PDLCs 在压力下会产生一系列促炎细胞因子,这些细胞因子有助于破骨细胞前体细胞的募集和破骨细胞的成熟。为了检查 GDF15 在此过程中的作用,使用 rGDF15 处理 PDLCs。随后的 RT-qPCR 分析表明,IL-6、IL-8 和 COX2 的表达在添加 GDF15 的 PDLCs 中增强。相反,当 GDF15 的表达被 siRNA 敲低时,这些炎症因子的力诱导上调明显受损。
在炎症因子中,RANKL 表达可以触发下游信号通路,而 OPG 是破骨细胞生成的负调控因子。RANKL/OPG 在 OTM 期间被上调并发挥关键作用。使用 rGDF15 处理 PDLCs,发现RANKL/OPG比值上调。相比之下,当 GDF15 表达被 siRNA 转染敲低时,压力诱导的 RANKL/OPG 上调明显减弱。总的来说,这些数据表明GDF15在压力诱导的炎症因子充分激活和RANKL/OPG中具有不可或缺的作用。
GDF15 促进 M1 样巨噬细胞极化
最近的研究报道称,压力可以诱导巨噬细胞向 M1 方向极化,这在 OTM 的破骨细胞分化中起重要作用。因此,实验研究了GDF15 是否参与巨噬细胞极化的调控。
为了阐明这一点,用 rGDF15 处理 RAW264.7 细胞。RT-qPCR结果显示,加入GDF15后M1标记基因IL-1β和IL-6表达增强,而M2标记基因Dectin表达降低,表明GDF15促进了RAW264.7中M1样巨噬细胞的极化。
GDF15 有助于在压力下激活 NF-κB 和 ERK 通路
接下来,开始探索 GDF15 促进促炎细胞因子表达的潜在机制。首先关注 NF-κB,它在细胞对机械刺激和破骨细胞分化的反应中发挥核心作用。GDF15 可能有助于 PDLCs 中 NF-κB 的激活,从而促进下游促炎基因的转录。为了验证这一点,在施加压力之前,在 PDLCs 中敲低GDF15,Western blot检测NF-κB在细胞核和细胞质中的分布变化。
结果显示,压力诱导NF-κB进入核。然而,当 GDF15 表达被抑制时,力诱导的 NF-κB 进入核的能力减弱,表现为细胞质中 NF-κB 增加,细胞核中NF-κB 减少。
巨噬细胞中的 NF-κB 活化对于破骨细胞分化很重要,因此检测了 GDF15 对 RAW264.7 细胞中 NF-κB 的影响。正如预期的那样,细胞核中 NF-κB 在 GDF15 处理的细胞中更丰富,而细胞质中 NF-κB 则相反。这些结果表明 GDF15 有助于力诱导的 NF-κB 激活。
除了 NF-κB,MAPK/ERK 是破骨细胞分化的另一个重要途径。实验假设 GDF15 也有助于力诱导的 ERK 激活。为了证明这一点,将 RAW264.7 细胞与用GDF15处理和压力处理后的PDLCs上清液共培养。Western blot分析显示,GDF15耗尽后,力诱导的ERK磷酸化水平降低。此外,GDF15 的施用还增强了ERK两个经典下游靶基因C-FOS和CCND1的表达。
这些数据共同验证了 GDF15 在调控 NF-κB 和 ERK 通路以响应压力中的作用。
GDF15 在 PDLCs 中受 YAP 调控
阐明了 GDF15 调控的信号通路后,研究人员试图描绘出负责力诱导的GDF15上调的上游信号分子。
YAP/TAZ 作为 Hippo 信号的重要节点,在机械转导过程中起着举足轻重的作用。由于YAP在乳腺癌细胞中抑制GDF15的表达,推测PDLCs中GDF15也可能受到YAP的负调控。用 YAP 抑制剂 Verteporfin 处理 PDLCs,发现 YAP 抑制后 GDF15 的蛋白质水平显著增加,这证实了 YAP 对 GDF15 的负调控作用。
此外,使用MST1/2 抑制剂 XMU-MP-1处理后,抑制了GDF15 的表达。由于 MST1/2 是内源性 MOB1、LATS1/2 和 YAP 磷酸化的激酶,它的抑制会导致 YAP 的激活。因此,这间接证明了 YAP 激活可以抑制 GDF15 的表达。
实验结论:
总之,该研究结果突出了GDF15是压力诱导破骨细胞分化的重要介质,从而为 OTM 期间 PDLCs 介导的破骨细胞生成的分子机制提供了新的见解。
参考文献:Li S, Li Q, Zhu Y, Hu W. GDF15 induced by compressive force contributes to osteoclast differentiation in human periodontal ligament cells. Exp Cell Res. 2020 Feb 1;387(1):111745. doi: 10.1016/j.yexcr.2019.111745. Epub 2019 Nov 22. PMID: 31765611.
原文链接:https://pubmed-ncbi-nlm-nih-gov.proxy.library.carleton.ca/31765611/
小编旨在分享、学习、交流生物科学等领域的研究进展。如有侵权或引文不当请联系小编修正。如有任何的想法以及建议,欢迎联系小编。感谢各位的浏览,更多资讯请关注公众号 Naturethink!

新鲁汶大学的公报指出,如今抗生素耐药菌的出现给人类和医药带来了新 ...

根据“生物安全关键技术研发”重点专项评审工作安排,生物中心将于2 ...

为更好的向用户、潜在用户提供我们的产品,即日起推出如下活动:凡向 ...

2018年度国家科学技术奖提名工作已结束,国家科学技术奖励工作办 ...

据英国《自然·通讯》杂志日前发表的一篇医学论文报告,科学家发现了 ...

Naturethink祝愿伟大祖国繁荣昌盛,欣欣向荣! ...

“免疫系统在高血压中扮演了未曾预料的重要角色。”英国格拉斯哥大学 ...

“来一场中国制造的品质革命!”3月5日,李克强总理在政府工作报告 ...

我司自主研发产品,重视知识产权,已拥有多项专利证书! ...

美国侨报网近日刊文称,一项新出炉的研究警告称,即使是失眠一夜,也 ...
公司完成细胞张应变与压力综合培养仪器的研发; ...

Naturethink网站及微信内容逐步完善,敬请查阅! ...

为提高区域自主创新能力,推进区域科技创新体系建设,加大创新驱动区 ...

2018年春节将至,我司放假时间安排为:2月14日至2月21日, ...

澳大利亚和英国一项研究显示,对于几乎任何年龄段的人群而言,快走都 ...

2018年国家自然科学基金项目申请工作已开始,你准备好了吗? ...
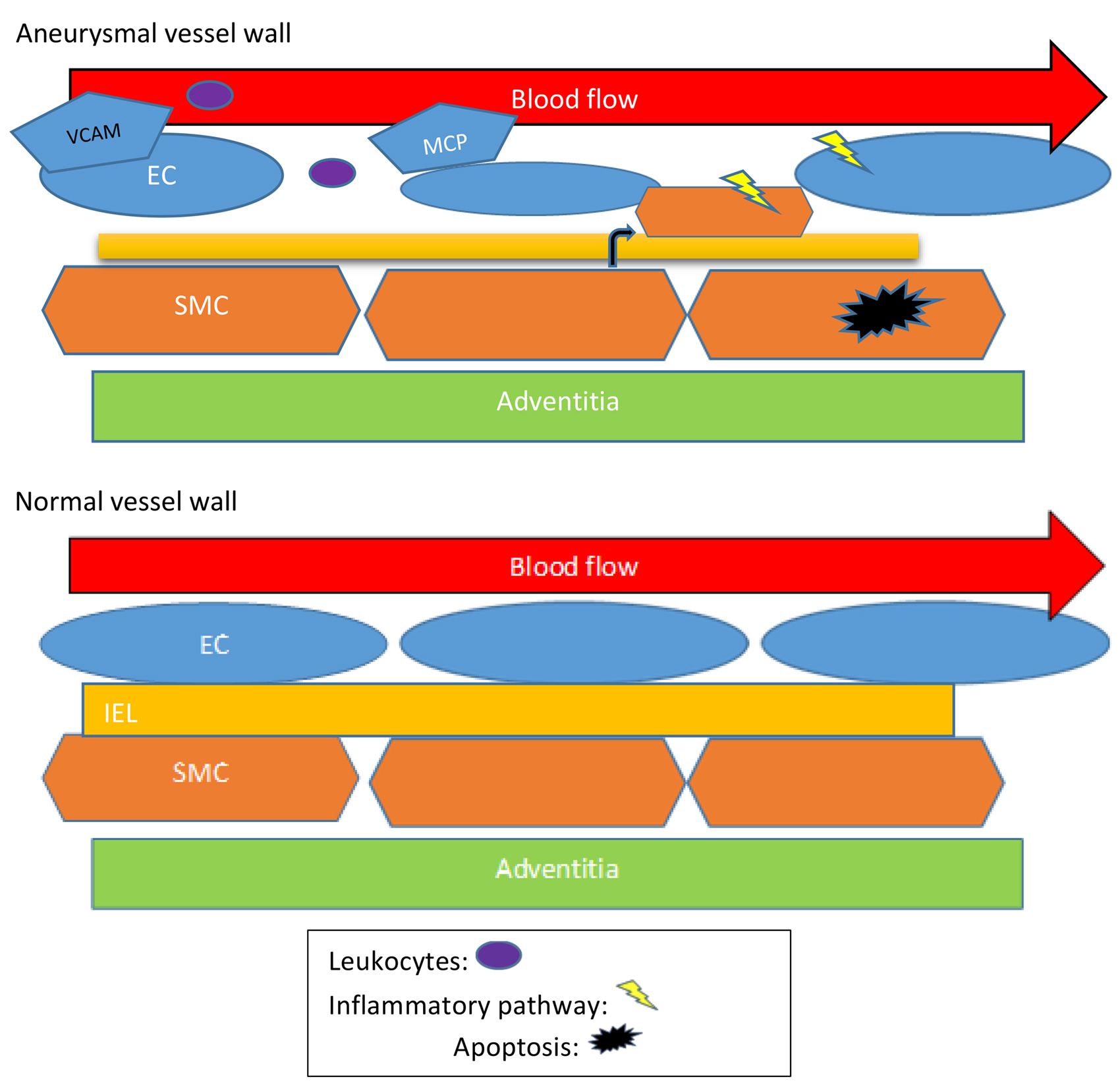
壁面剪切应力(WSS),是单位面积上由血管表面流动的液体产生的接 ...
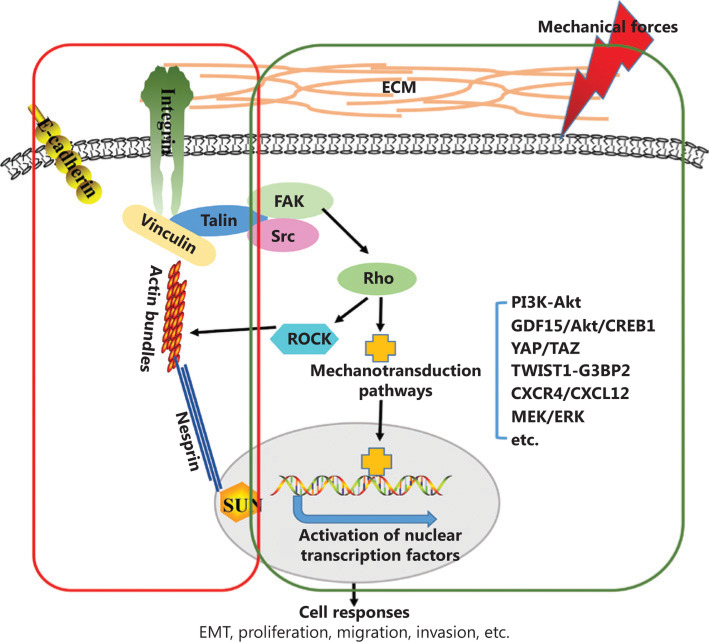
癌症在促进肿瘤表型表观遗传重编程和修饰的复杂组织微环境中发展。此 ...