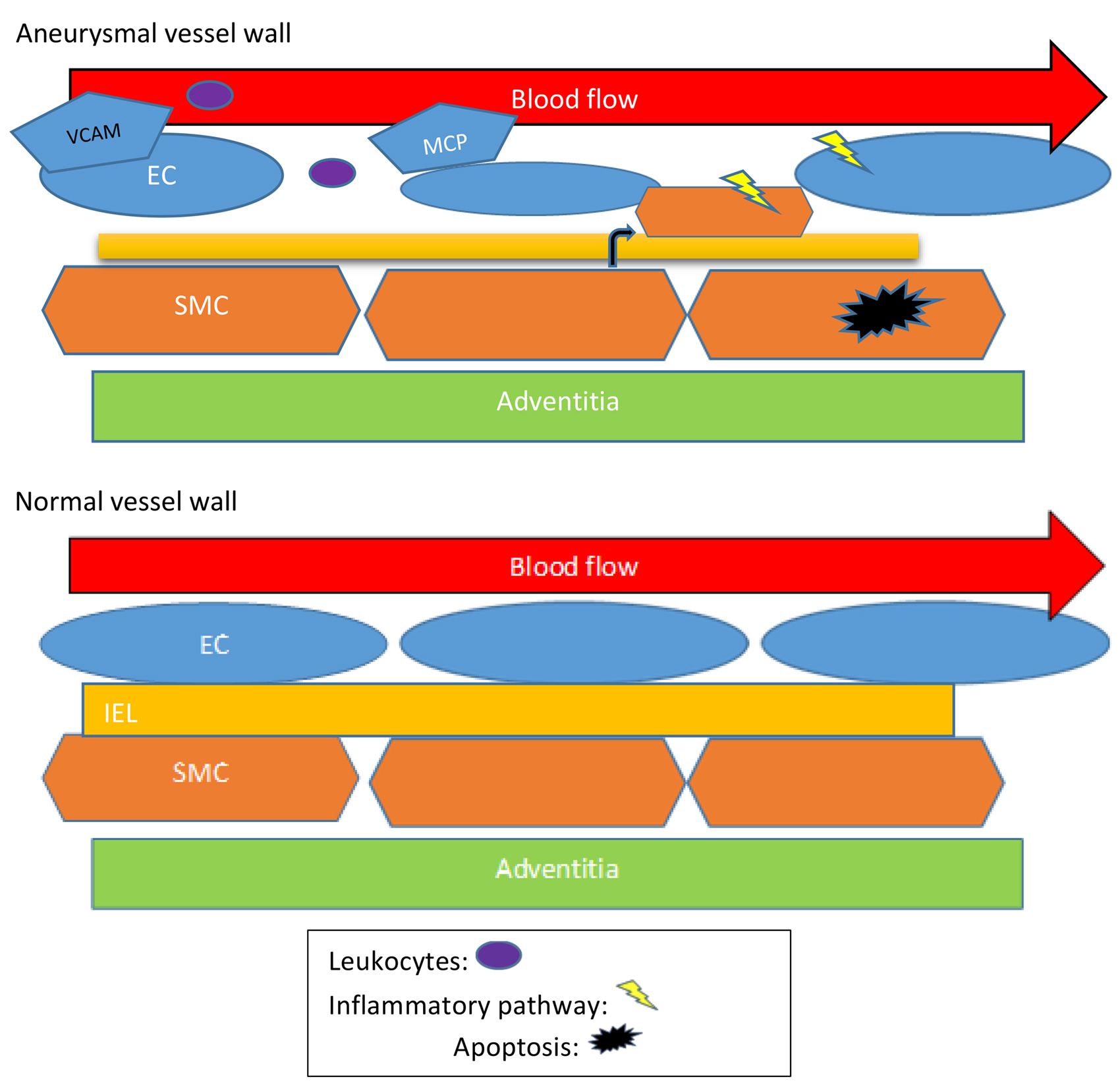
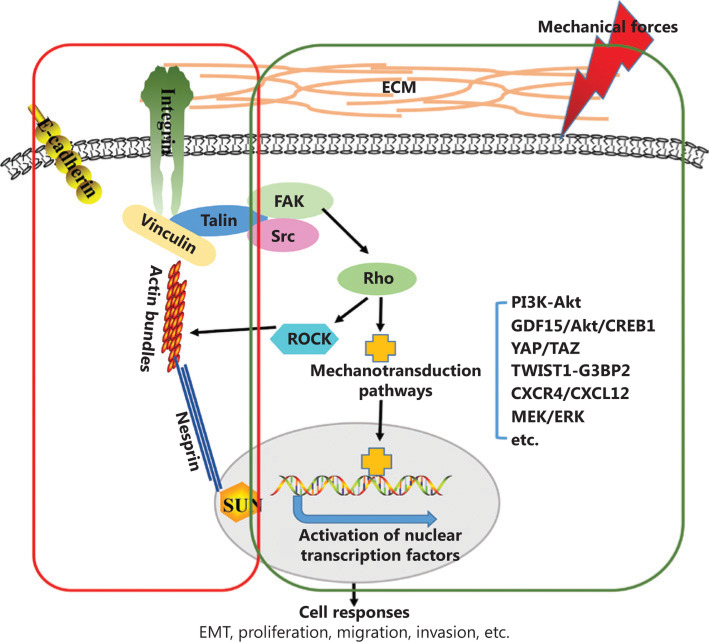
内皮糖萼由糖胺聚糖组成,包括透明质酸(HA)、硫酸乙酰肝素、硫酸软骨素和唾液酸,是一种位于内皮细胞顶端表面的糖蛋白复合物。该层有助于血管壁的屏障特性,并参与机械感应和剪切力到内皮的转导。
剪切应力是指血流与血管内皮间摩擦力。高剪切应力(HSS,12-15 dyn/cm2)已被证明可以维持内皮糖萼的完整性并抵抗早期动脉粥样硬化病变的发展。然而,低剪切应力(LSS,<5 dyn/cm2 )也被认为通过减少内皮糖萼的尺寸在早期动脉粥样硬化中起关键作用。
研究发现,LSS 通过透明质酸酶2(HYAL2)途径降解内皮糖萼内的 HA,并进一步证明 LSS 诱导的糖萼损伤导致 eNOS-Ser633 去磷酸化并减少 NO 产生。然而,LSS 如何激活 HYAL2 仍不清楚。Na + -H +交换剂 (NHE)1 催化细胞内 (H + ) 离子的排出以交换细胞外 (Na + ) 离子,是可能的候选者之一,并且是一种普遍存在的膜蛋白,可调节细胞 pH 值。有研究发现, NHE1 被激活以产生酸性细胞外微环境,导致 HYAL2 在人乳腺肿瘤细胞中激活。据报道,在内皮细胞中,HSS 可引发 AMPK 磷酸化并增加 AMPK 的活性,AMPK 在调节细胞内 pH 值中起重要作用。AMPK 是否通过细胞外基质的 NHE1 酸化参与 LSS 诱导的 HYAL2 活化仍有待确定。因此,南京医科大学南京第一医院心内科的专家学者进行了研究,使用功能丧失方法和 AMPKα、NHE1 和 HYAL2 的激活或失活,旨在确定 LSS 诱导的内皮糖萼损伤和早期内皮炎症对 LSS 的影响和分子机制。文章为《 AMP-activated protein kinase regulates glycocalyx impairment and macrophage recruitment in response to low shear stress.》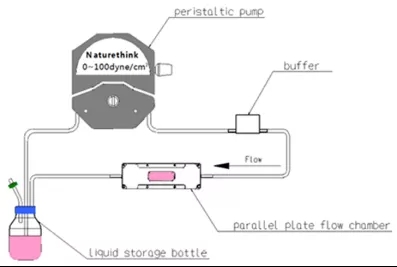
实验中的 LSS 为 2 dyn/cm2,HSS 为 15 dyn/cm2。
NHE1 介导 LSS 诱导的糖萼损伤
LSS 激活 NHE1 的机制,是否涉及 AMPK,以及 NHE1 在 LSS 诱导的糖萼损伤中的作用尚不清楚。实验首先在细胞经受 LSS 5、15、30 和 60 min 后检查了 NHE1 蛋白及其磷酸化以及 NHE1 的活性。未经 LSS 处理的细胞用作对照。
如图1 A,尽管表面 NHE1 蛋白表达没有显著变化,但在 LSS 暴露 15 min 后,NHE1 磷酸化水平显著升高,在 30 min 时达到最高水平。NHE1 活性早在 LSS 处理后 15 min 就增强并持续至少 60 min。为了确认 NHE1 活性对响应 LSS 的糖萼损伤的影响,在 LSS 暴露之前,用编码显性阴性形式的酶 (AdDN-NHE1) 的腺病毒转导 HUVECs,或用靶向 NHE1 活性的 cariporide(卡立泊来德)预处理。使用 AdDN-NHE1 抑制 NHE1 活性显著降低了 LSS 诱导的 NHE1 磷酸化和 NHE1 活性。除了 AdDN-NHE1 外,cariporide 也可抑制 NHE1 活性。接下来,使用 AFM 检查内皮糖萼厚度(GCT)。糖萼的最大厚度为 628 nm。LSS 显著稀释了内皮糖萼,然而,使用 AdDN-NHE1 可抑制 NHE1 活性,或 cariporide 保护糖萼免受 LSS 诱导的 GCT 降低。
AMPK 调节 NHE1 依赖性糖萼损伤以响应 LSS实验显示了 AMPKα 在其激活位点 Thr172 磷酸化的下调,伴随着 AMPK 活性的降低,这在 LSS 处理后 15 min 就很明显,并且持续了至少 60 min。相反,AMPKα 蛋白表达无明显变化。为了检查 AMPK 的失活是否介导 LSS 诱导的 NHE1 活化和糖萼降解,在没有或存在 AMPK 激活剂 ampkinone 的情况下,将 HUVECs 暴露于 LSS 30 min。在接受 30 min LSS 的细胞中,用 ampkinone 处理恢复了 AMPKα-Thr172 磷酸化水平以及被 LSS 下调的 AMPK 活性。Ampkinone 处理还阻止了响应 LSS 的 NHE1 磷酸化和 NHE1 活性的增加。
在平行实验中,在 LSS 暴露前 30 min 用 AdCA-AMPKα 转导 HUVECs。组成型活性 AMPKα 不仅恢复了由 LSS 抑制的 AMPK 活性,而且减弱了 LSS 诱导的 NHE1 磷酸化和 NHE1 活化。然而,使用 AdDN-NHE1 抑制 NHE1 活性既不会减弱 AMPKα-Thr172 去磷酸化,也不会逆转 LSS 诱导的 AMPK 失活。
接下来研究了 AMPK 在 LSS 诱导的 HUVECs 糖萼损伤中的作用。HUVECs 与 AMPK 激活剂 ampkinone 的孵育显著减弱了 LSS 诱导的糖萼损伤。为了进一步证实 AMPK 活性对 LSS 下内皮糖萼损伤的影响,在 HUVECs 中表达了 AdDN-AMPKα 或 AdCA-AMPKα。观察到 AdCA-AMPKα 保护糖萼免受 LSS 诱导的损伤。然而,AdDN-AMPKα 显著逆转了 HSS 诱导的糖萼保护。图3 C显示 cariporide、ampkinone、AdDN-NHE1 和 AdCA-AMPKα 显著阻止糖萼中 HA 表达降低和糖萼变薄以响应 LSS。这些结果表明 LSS 引起的 AMPK 失活介导了内皮糖萼损伤。
之前的研究表明,HYAL2 参与了响应 LSS 的糖萼损伤。在该实验中,研究人员证实了 LSS 激活 HYAL2 降解内皮糖萼。上述结果表明,LSS 诱导的内皮糖萼降解起因于 AMPK 失活和 NHE1 活化(图1-3)。实验接下来研究了 AMPK 和 NHE1 对 LSS 刺激的 HUVECs 中 HYAL2 活化的作用。结果发现,AMPK 和 NHE1 轴调控 LSS 诱导的 HYAL2 活化。最后,实验证明 Ampkinone 处理可防止 LSS 诱导的左颈总动脉狭窄小鼠糖萼尺寸减少,并且保护内皮糖萼延缓左颈总动脉狭窄小鼠内皮炎症的发展。
总之,这项研究的结果表明,暴露于 LSS 的内皮细胞中 AMPK 的去磷酸化可能有助于 NHE1 的激活。后者被认为是一种离子通道蛋白,催化细胞内(H +) 离子和下调细胞外 pH 值。酸活性 HYAL2 降解内皮糖萼中的 HA,导致内皮糖萼变薄。实验进一步发现糖萼损伤导致粘附分子 VCAM-1 和 ICAM-1 的表达增加,以及巨噬细胞募集到左颈动脉-PL 小鼠的内皮细胞。因此,特定的糖萼保存,例如通过刺激 AMPK,可能是一种预防早期内皮炎症和抑制动脉粥样硬化病变形成的新策略。参考文献:Zhang J, Kong X, Wang Z, Gao X, Ge Z, Gu Y, Ye P, Chao Y, Zhu L, Li X, Chen S. AMP-activated protein kinase regulates glycocalyx impairment and macrophage recruitment in response to low shear stress. FASEB J. 2019 Jun;33(6):7202-7212. doi: 10.1096/fj.201801869RRR. Epub 2019 Mar 12. PMID: 30860864.原文链接:https://pubmed-ncbi-nlm-nih-gov.proxy.library.carleton.ca/30860864/
小编旨在分享、学习、交流生物科学等领域的研究进展。如有侵权或引文不当请联系小编修正。如有任何的想法以及建议,欢迎联系小编。
标签: