缺血性心脏病 (IHD) 是全世界死亡的主要原因之一。冠状动脉旁路移植术 (CABG) 仍然是治疗复杂的冠状动脉疾病、糖尿病和心室功能低下的主要手段。长隐静脉 (LSV) 是许多患者最常用的导管,但是,由于内膜增生 (IH) 和动脉粥样硬化的发展,晚期狭窄或闭塞的发生率相当高,使其使用复杂化。
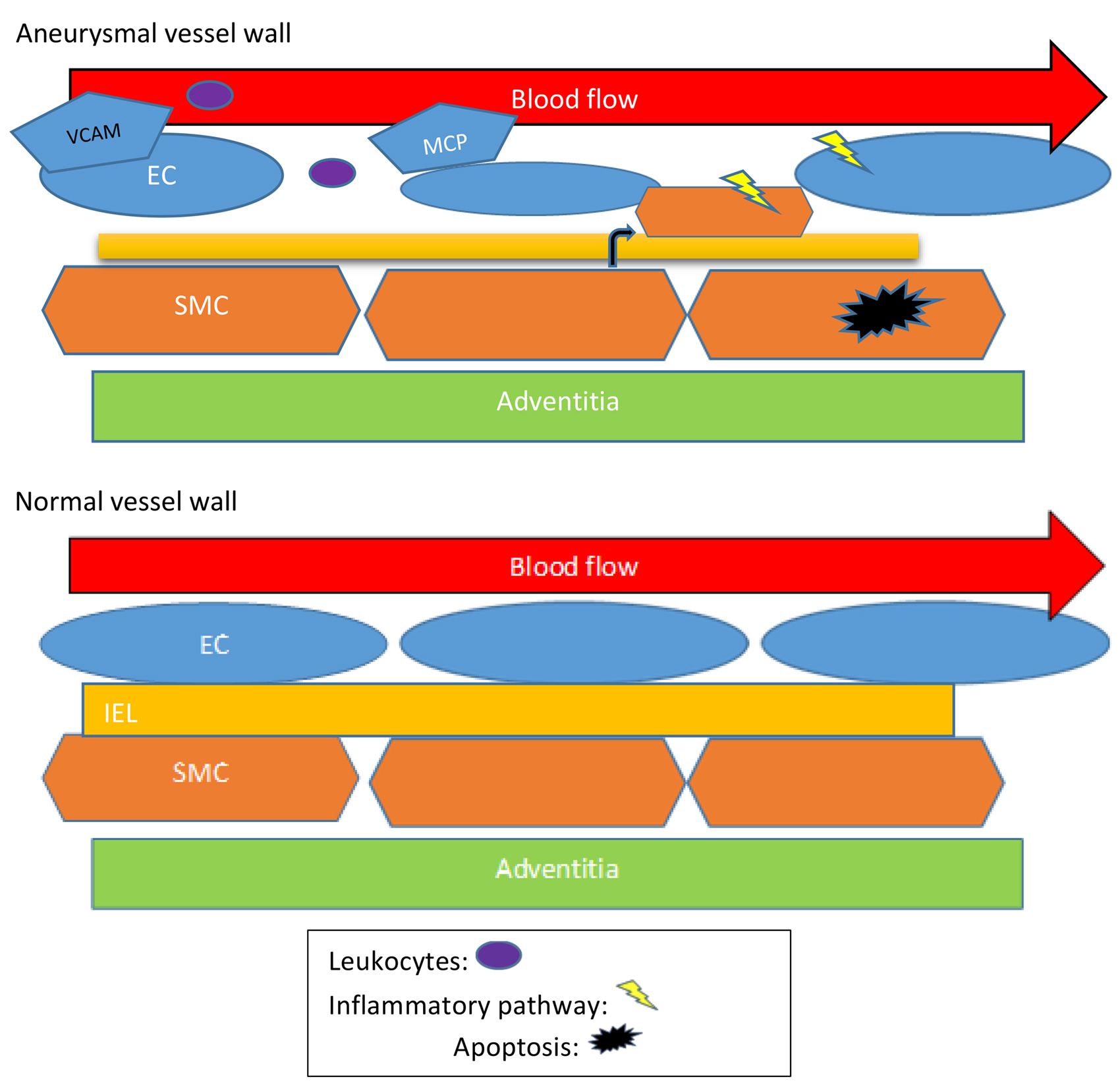
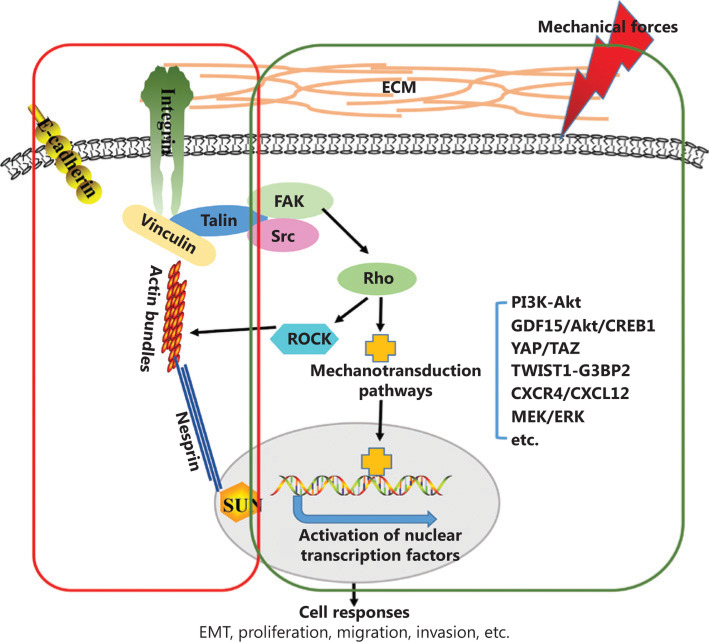
IH 是一种慢性炎症过程,从内皮细胞 (EC) 激活开始,随后平滑肌细胞 (SMC) 向内膜迁移和增殖,然后伴随着细胞外基质 (ECM) 的改变。血管炎症受信号中介的调控,包括核因子-κB、NF-κB (p65),它们触发EC的趋化因子如单核细胞趋化蛋白-1 (CCL2) 和其他促炎分子的表达。血管对炎症过程的易感性可能在一定程度上与它们产生的血管床和它们长期暴露的血液动力学环境类型有关。原位静脉内皮细胞适应慢性低剪切应力水平,并且在移植后,它们暴露于动脉系统中高达十倍的剪切应力。已知急性发作的剪切应力增加率会改变静脉EC的表型;然而,支持这种反应的机制尚未完全阐明。为了更好地了解静脉对移植的促炎反应的内在分子机制,来自英国布里斯托大学医学院、英国谢菲尔德大学感染、免疫和心血管疾病系的专家学者进行了合作研究,于 Scientific Reports 发表了联合撰写的研究成果《NF-κB inhibition prevents acute shear stress-induced inflammation in the saphenous vein graft endothelium》。该实验在体外、体内研究了急性剪切变化对 NF-κB 活化和相关静脉内皮细胞 (vECs) 反应的影响。
实验结果
1.急性动脉壁面剪切应力(WSS)在体外诱导 LSV ECs 的促炎反应
新鲜获得的人LSV片段在离体时,急性暴露于动脉剪切应力 (12dyn /cm2),在体外静脉旁路移植模型中,这一速率先前被认为与EC激活和血管重塑有关。实验观察到在暴露于急性高剪切应力 (急性动脉WSS) 后,LSV ECs 中 CCL2 mRNA 水平显著升高。En face 免疫荧光染色显示,静脉暴露于急性动脉WSS 增加了 ECs 中 CCL2 的蛋白表达。
2.抑制 NF-κB 阻止了 LSV 内皮中对急性动脉 WSS 的促炎反应
为了研究 NF-κB 的可能作用,实验分析了在暴露于动脉剪切应力下 LSVs 中的 p65 NF-kB子单位的表达。急性动脉 WSS 增强了内皮细胞中 p65 的核易位,表明急性动脉剪切应力激活了 LSV 内皮细胞中的 NF-kB。为了研究 NF-κB 在急性动脉 WSS 的促炎反应中的功能,实验使用了选择性小分子 NF-κB 抑制剂 BAY11-7085 (BAY)。50 µmol/L BAY 预处理的 LSV 通过降低 CCL2 水平来调节 EC 对急性动脉 WSS 的反应。此外,抑制 NF-κB 减少了急性动脉 WSS 诱导的单核细胞粘附到 LSV 内皮细胞。因此可以得出结论,抑制 NF-κB 可以阻止急性动脉 WSS 下静脉内单核细胞与内皮细胞的粘附启动。
3.急性动脉 WSS 在体外激活促炎反应和 NF-κB 经典通路
为了验证体外研究结果并进一步研究涉及静脉 EC 对动脉剪切应力速率反应的分子基础,研究人员在体外研究了急性动脉 WSS 对 HUVECs 的影响。
急性高剪切应力显著增加了 p65 的核易位,这与 IκBα 表达的反向降低有关,表明 NF-κB 经典通路被激活。此外,在急性动脉 WSS 持续 30 分钟后,NF-κB 在丝氨酸残基 276 (Ser-276) 处被磷酸化,同时还显示出与 NF-κB 共有寡核苷酸的 DNA 结合增加,两者都表明 NF-κB 的转录激活。这种转录激活是短暂的,在 30 分钟时达到峰值,这可能表明在 60 分钟急性动脉 WSS 暴露后,IκBα 对 NF-κB 负调控的前馈机制。实验观察到急性动脉 WSS,但不是低剪切力,与 CCL2 的上调有关。使用 20 μmol/L BAY 预处理抑制 NF-κB 经典通路导致促炎激活减少,与体外观察到的结果相似。通过腺病毒介导的 WT-IκBα 过表达进一步验证了这些发现,这表明 WT-IκBα 过表达可抑制急性动脉 WSS 诱导的 CCL2 。此外,免疫分析显示,与静态对照相比,急性动脉 WSS 4小时后,CCL2 的表达显著降低。同时,WT-IκBα 的过表达防止了急性动脉 WSS 暴露后 VE-钙粘蛋白细胞间接触的丢失,表明内皮屏障完整。接下来,实验研究了在体外动态和实时检测下,暴露于急性动脉WSS 后,NF-κB 抑制对单核细胞- EC 相互作用的影响。结果显示,用 20 μmol/L BAY 预处理 HUVECs 显著降低了急性动脉 WSS 诱导的动态单核细胞与 vEC 单层的粘附。
实验结论
在这里,实验表明 NF-κB 经典通路在 LSV 的内皮细胞中被激活,以响应急性暴露于动脉剪切应力速率,并且该通路是静脉血管炎症的关键调节剂。体外实验进一步证明,在急性血流诱导之前靶向 NF-κB 足以防止内皮细胞 CCL2 表达和单核细胞募集,以及 EC 细胞-细胞间接触中断,这是内皮功能障碍的另一个标志。总之,实验确定急性动脉 WSS 负责 LVG EC 的早期促炎激活,该过程受 NF-κB(p65)激活调节,导致促炎介质上调和单核细胞募集增加,因此,这为NF-κB参与静脉移植内皮中剪切诱导的炎症机制提供了一个证据。参考文献:Ward AO, Angelini GD, Caputo M, Evans PC, Johnson JL, Suleiman MS, Tulloh RM, George SJ, Zakkar M. NF-κB inhibition prevents acute shear stress-induced inflammation in the saphenous vein graft endothelium. Sci Rep. 2020 Sep 15;10(1):15133. doi: 10.1038/s41598-020-71781-6. PMID: 32934266; PMCID: PMC7492228.原文链接:https://pubmed-ncbi-nlm-nih-gov.proxy.library.carleton.ca/32934266/小编旨在分享、学习、交流生物科学等领域的研究进展。如有侵权或引文不当请联系小编修正。如有任何的想法以及建议,欢迎联系小编。感谢各位的浏览,更多资讯请关注公众号 Naturethink!
标签: